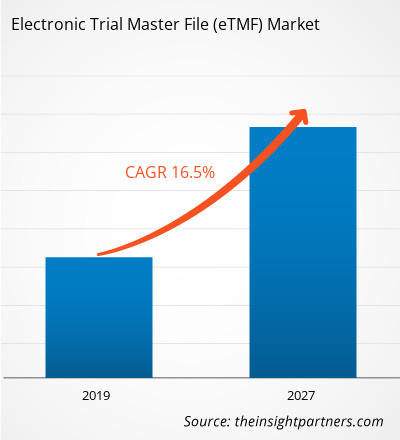
[تقرير بحثي] تم تقييم ملف التجارب الإلكترونية الرئيسي في سوق الرعاية الصحية بمبلغ 938.32 مليون دولار أمريكي في عام 2018 ومن المتوقع أن يصل إلى 3،155.64 مليون دولار أمريكي بحلول عام 2027؛ ومن المتوقع أن ينمو بمعدل نمو سنوي مركب قدره 16.5٪ من عام 2019 إلى عام 2027.
يمكن تعريف أنظمة الملفات الرئيسية للتجارب الإلكترونية (eTMF) بأنها تكامل بين مكونات البرامج والأجهزة المسؤولة بشكل جماعي عن الإدارة المثلى لبيانات التجارب السريرية. تساعد هذه الحلول في تبسيط البيانات التي تم إنشاؤها أثناء سير التجربة السريرية في تنسيق رقمي سهل التخزين، والذي يمكن استرجاعه من قبل مستخدمين مختلفين مما يفيد في سهولة الوصول وتقليل التكلفة المرتبطة بعمليات صيانة البيانات الإدارية واليدوية في التجارب السريرية. يُعزى نمو سوق الملفات الرئيسية للتجارب الإلكترونية في الرعاية الصحية إلى الزيادة في عدد التجارب السريرية، وزيادة انتشار الأمراض والتقدم التكنولوجي الذي عزز السوق على مر السنين. ومع ذلك، من المرجح أن يكون لنقص المهنيين المهرة تأثير سلبي على نمو السوق في السنوات القادمة. من ناحية أخرى، من المرجح أن توفر المبادرات الاستراتيجية المتزايدة من قبل اللاعبين في السوق فرص نمو على مدى السنوات القادمة.
من المتوقع أن يشهد ملف التجارب الإلكترونية الرئيسي في سوق الرعاية الصحية نموًا كبيرًا بعد الوباء. لقد أثرت جائحة كوفيد-19 على الاقتصادات والصناعات في مختلف البلدان بسبب عمليات الإغلاق وحظر السفر وإغلاق الأعمال. لقد أثقلت أزمة كوفيد-19 كاهل أنظمة الصحة العامة في العديد من البلدان وسلطت الضوء على الحاجة القوية للاستثمار المستدام في أنظمة الصحة. مع تقدم جائحة كوفيد-19، من المتوقع أن تشهد صناعة الرعاية الصحية انخفاضًا في النمو. يزدهر قطاع العلوم الحيوية بسبب زيادة الطلب على منتجات التشخيص المختبري وارتفاع أنشطة البحث والتطوير في جميع أنحاء العالم. ومع ذلك، يشهد قطاع التقنيات الطبية والتصوير انخفاضًا في المبيعات بسبب عدد أقل من العمليات الجراحية التي يتم إجراؤها وتأخير أو إطالة شراء المعدات. بالإضافة إلى ذلك، من المتوقع أن تصبح الاستشارات الافتراضية من قبل المتخصصين في الرعاية الصحية نموذج تقديم الرعاية السائد بعد الوباء. مع تحويل التطبيب عن بعد لتقديم الرعاية، ستستمر الصحة الرقمية في الازدهار في السنوات القادمة. بالإضافة إلى ذلك، من المتوقع أيضًا أن تمهد التجارب السريرية المعطلة والتأخير اللاحق في إطلاق الأدوية الطريق للتجارب الافتراضية بالكامل في المستقبل. ومن المتوقع ظهور تقنيات جديدة مثل mRNA وتغيير صناعة الأدوية، ومن المتوقع أيضًا أن يشهد السوق المزيد من التكامل الرأسي والمشاريع المشتركة في السنوات القادمة.
قم بتخصيص هذا التقرير ليناسب متطلباتك
ستحصل على تخصيص لأي تقرير - مجانًا - بما في ذلك أجزاء من هذا التقرير، أو تحليل على مستوى الدولة، وحزمة بيانات Excel، بالإضافة إلى الاستفادة من العروض والخصومات الرائعة للشركات الناشئة والجامعات
- احصل على أهم اتجاهات السوق الرئيسية لهذا التقرير.ستتضمن هذه العينة المجانية تحليلاً للبيانات، بدءًا من اتجاهات السوق وحتى التقديرات والتوقعات.
رؤى السوق
التطبيقات المتنامية لملفات المحاكمة الإلكترونية الرئيسية في الرعاية الصحية لدفع نمو سوق ملفات المحاكمة الإلكترونية الرئيسية في الرعاية الصحية
إن البحث والتطوير يشكلان جزءًا مهمًا وأساسيًا من أعمال الشركة. إن عمليات صناعة الأدوية لها تأثيرات اجتماعية واقتصادية كبيرة على المجتمع في شكل استثمارات في البحث والتطوير والتصنيع. إن البحث والتطوير هو "العمود الفقري" لأي نظام اكتشاف للأدوية لتحقيق النجاح، كما أن ملف التجارب الإلكترونية الرئيسي هو برنامج أساسي في البحث والتطوير للكيانات العلاجية الجديدة القائمة على الأدوية والتكنولوجيا الحيوية. تركز شركات الأدوية والتكنولوجيا الحيوية بشكل أساسي على البحث والتطوير للتوصل إلى جزيئات جديدة لتطبيقات علاجية مختلفة ذات إمكانات طبية وتجارية كبيرة. تستثمر الشركات بشكل رئيسي في البحث والتطوير بهدف تقديم منتجات عالية الجودة ومبتكرة إلى السوق. على سبيل المثال، زاد الإنفاق العالمي على البحث والتطوير في عام 2017 بنسبة 3.9 في المائة إلى 165 مليار دولار مقارنة بعام 2016. كما زاد متوسط الإنفاق على البحث والتطوير بشكل معتدل إلى 20.9 في المائة كنسبة مئوية من إجمالي مبيعات الوصفات الطبية. بالإضافة إلى ذلك، ووفقًا لمسح سنوي لأعضاء جمعية PhRMA في عام 2017، أفادت شركات الأدوية بإنفاق 71.4 مليار دولار على البحث والتطوير.
استثمرت شركات الأدوية المزيد في البحث والتطوير لتكثيف عملية التجارب السريرية. على سبيل المثال، اعتبارًا من 30 يونيو 2019، شقت شركة أسترازينيكا الطريق بإنفاق 25.63٪ من إيراداتها على البحث والتطوير، واعتبارًا من 31 مارس 2019، أنفقت شركة إيلي ليلي 22.38٪ من إيراداتها على البحث والتطوير، واعتبارًا من 30 يونيو 2019، لم تكن شركة روش هولدينج إيه جي بعيدة عن الركب حيث أنفقت 21.29٪ على البحث والتطوير.
إن نفقات البحث والتطوير عادة ما تتكبد أثناء عمليات اكتشاف واختبار وتطوير المنتجات الجديدة، والدفعات المقدمة، وإتمام المراحل المهمة، وتحسين النتائج الحالية، فضلاً عن إثبات فعالية المنتج والامتثال التنظيمي قبل إطلاقه. وعلاوة على ذلك، نمت الاستثمارات في البحث والتطوير من قبل شركات الأدوية في الولايات المتحدة بشكل ثابت على مدى السنوات الخمس عشرة الماضية.
إن تطوير واكتشاف الأدوية عملية تستغرق وقتًا طويلاً ومكلفة. فالعملية من الاكتشاف المبكر أو التصميم إلى التطوير إلى الموافقة التنظيمية قد تستغرق أكثر من 10 إلى 15 عامًا. وخلال مرحلة تطوير مادة دوائية، تكون هناك حاجة إلى خدمات اختبار مختلفة للتحقق من جودة المنتج وفعاليته. وبالتالي، تفضل شركات الأدوية والتكنولوجيا الحيوية حفظ البيانات في ملف رئيسي إلكتروني لتوفير التكلفة والوقت، وهو ما يُتوقع أن يدفع نمو السوق.
تُعَد التجارب السريرية واحدة من أهم الخطوات وأكثرها أهمية في اكتشاف الأدوية سواء كان العلاج أو الاستراتيجية الطبية أو الجهاز آمنًا وفعالًا للاستخدام البشري أو البيطري. تساعد الدراسات السريرية في فهم وتحديد أفضل الأساليب للعلاج في مجالات علاجية معينة. تُجرى التجارب السريرية خصيصًا لجمع البيانات حول سلامة وفعالية تطوير منتج وأداة جديدة. قبل أن توافق السلطات التنظيمية على جزيئات الدواء والأجهزة الطبية، يتم إجراء سلسلة من الدراسات السريرية. يؤدي الانتشار المتزايد لمختلف الأمراض المعدية وغير المعدية إلى زيادة الطلب على تطوير أدوية أو أجهزة طبية جديدة للعلاج. ومن المتوقع أن يؤدي هذا بدوره إلى زيادة الطلب على أنشطة التجارب السريرية لمختلف المجالات العلاجية.
تهدف شركات الأدوية الحيوية والصيدلانية المشاركة في التجارب السريرية إلى التحول من أنظمة إدارة المستندات الورقية في خزائن الملفات إلى أنظمة إدارة المستندات الإلكترونية حيث يتم تخزين المستندات في أرشيفات إلكترونية عبر الإنترنت. من خلال تنفيذ نظام eTMF شامل يسمح للمؤسسات بأتمتة مستندات TMF وتسجيلها وإدارتها وتسجيل المخاطر غير الضرورية ويمكنها غالبًا تحقيق وفورات في تكاليف التجارب السريرية مقارنة بعمليات التعامل اليدوي مع الورق.
من المرجح أن يؤدي ارتفاع معدل تبني نظام الملفات الرئيسية للتجارب الإلكترونية في العملية السريرية إلى تعزيز السوق. على سبيل المثال، يعد NextDocs من Aurea Software منتدى للملفات الرئيسية للتجارب الإلكترونية (eTMF) للتعاون السريري في إدارة سجلات التجارب السريرية. إنه نظام إدارة محتوى لصناعة الأدوية يوفر وسيلة رسمية لتنظيم وتخزين المستندات والصور والمحتوى الرقمي الآخر للتجارب السريرية الصيدلانية التي قد تكون مطلوبة للامتثال للهيئات التنظيمية الحكومية. في التجارب السريرية، تدعم EMA بشكل كامل استخدام أنظمة eTMF للتخزين الإلكتروني كبديل للورق. تستشهد الوكالة بمشاكل الجودة في TMFs وeTMFs في بيان تحذيري بسبب محتوى الورق والتناقضات مثل الصفحات المفقودة أو العلامات غير المناسبة أو المستندات غير المكتملة. نظرًا للميزات المبتكرة لـ eTMF مثل مركزية وإدارة توثيق التجارب السريرية وقدرات البحث القوية (مع البيانات الوصفية) والطرق المتعددة لإضافة المستندات، أصبح eTMF مهمًا لكفاءة الأعمال وتوفير التكاليف واختصار الجداول الزمنية لإنتاج منتجات BioPharma لتنفيذ عمليات إدارة المستندات الإلكترونية. إن السر في تقديم أطر عمل eTMF المتوافقة هو استخدام نموذج محتوى مشترك؛ ومعايير تعتمد على المفردات؛ وتقنيات المعايير المعتمدة على الويب.
بسبب التقدم في تحويل ملف التجارب الرئيسي إلى ملف التجارب الرئيسي الإلكتروني، تتبنى منظمة أبحاث العقود وشركات الأدوية والتكنولوجيا الحيوية ملف التجارب الرئيسي الإلكتروني لتحسين إدارة البيانات السريرية وعملية إدارة التجارب السريرية. وترجع الأسباب والعوامل المذكورة أعلاه إلى تعزيز نمو سوق ملف التجارب الرئيسي الإلكتروني.
رؤى قائمة على المكونات
من حيث المكونات، يتم تقسيم ملف المحاكمة الإلكتروني الرئيسي في سوق الرعاية الصحية إلى الخدمة والبرمجيات. احتل قطاع الخدمة الحصة الأكبر من السوق في عام 2019.
رؤى تعتمد على طريقة التسليم
استنادًا إلى طريقة التسليم، يتم تقسيم ملف إدارة التجارب الإلكترونية في سوق الرعاية الصحية إلى ملف إدارة التجارب الإلكترونية المستند إلى السحابة وملف إدارة التجارب الإلكترونية المحلي. احتلت شريحة ملف إدارة التجارب الإلكترونية المستند إلى السحابة الحصة الأكبر من السوق في عام 2019.
رؤى تعتمد على المستخدم النهائي
من حيث المستخدم النهائي، يتم تقسيم ملف الاختبار الإلكتروني في سوق الرعاية الصحية إلى شركات الأدوية والتكنولوجيا الحيوية، وشركات كروس وغيرها. احتلت شريحة شركات الأدوية والتكنولوجيا الحيوية الحصة الأكبر من السوق في عام 2019.
يتبنى اللاعبون في سوق الرعاية الصحية في مجال الملفات الرئيسية للتجارب الإلكترونية استراتيجيات إطلاق المنتجات وتوسيع نطاقها لتلبية متطلبات العملاء المتغيرة في جميع أنحاء العالم، مما يسمح لهم أيضًا بالحفاظ على اسم علامتهم التجارية عالميًا.
رؤى إقليمية حول سوق الملفات الرئيسية للمحاكمة الإلكترونية (eTMF)
لقد قام المحللون في Insight Partners بشرح الاتجاهات والعوامل الإقليمية المؤثرة على سوق الملفات الرئيسية للمحاكمة الإلكترونية (eTMF) طوال فترة التوقعات بشكل شامل. يناقش هذا القسم أيضًا قطاعات سوق الملفات الرئيسية للمحاكمة الإلكترونية (eTMF) والجغرافيا في جميع أنحاء أمريكا الشمالية وأوروبا ومنطقة آسيا والمحيط الهادئ والشرق الأوسط وأفريقيا وأمريكا الجنوبية والوسطى.
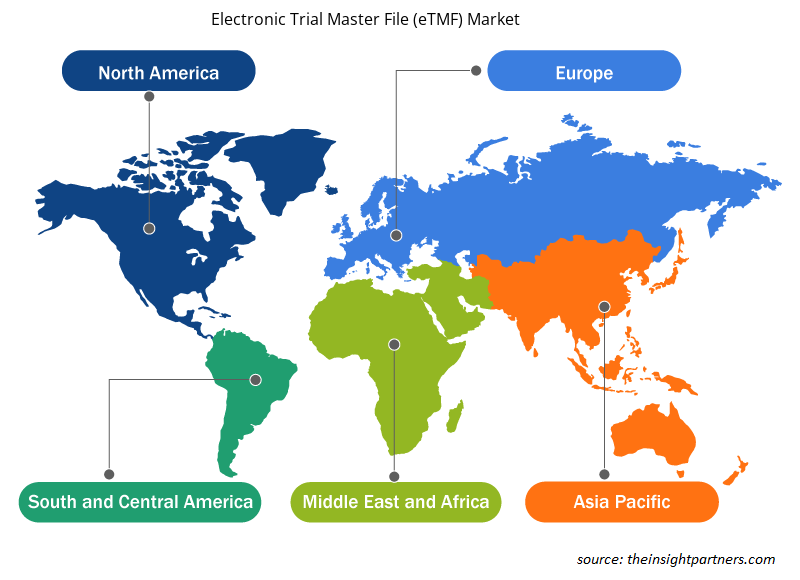
- احصل على البيانات الإقليمية المحددة لسوق الملفات الرئيسية للمحاكمة الإلكترونية (eTMF)
نطاق تقرير سوق الملفات الرئيسية للمحاكمة الإلكترونية (eTMF)
| سمة التقرير | تفاصيل |
|---|---|
| حجم السوق في عام 2018 | 938.32 مليون دولار أمريكي |
| حجم السوق بحلول عام 2027 | 3,155.64 مليون دولار أمريكي |
| معدل النمو السنوي المركب العالمي (2018 - 2027) | 16.5% |
| البيانات التاريخية | 2016-2017 |
| فترة التنبؤ | 2019-2027 |
| القطاعات المغطاة | حسب المكون
|
| المناطق والدول المغطاة | أمريكا الشمالية
|
| قادة السوق وملفات تعريف الشركات الرئيسية |
|
كثافة اللاعبين في سوق الملفات الرئيسية للمحاكمة الإلكترونية (eTMF): فهم تأثيرها على ديناميكيات الأعمال
يشهد سوق الملفات الرئيسية للتجارب الإلكترونية (eTMF) نموًا سريعًا، مدفوعًا بالطلب المتزايد من المستخدم النهائي بسبب عوامل مثل تفضيلات المستهلك المتطورة والتقدم التكنولوجي والوعي المتزايد بفوائد المنتج. ومع ارتفاع الطلب، تعمل الشركات على توسيع عروضها والابتكار لتلبية احتياجات المستهلكين والاستفادة من الاتجاهات الناشئة، مما يؤدي إلى زيادة نمو السوق.
تشير كثافة اللاعبين في السوق إلى توزيع الشركات أو المؤسسات العاملة في سوق أو صناعة معينة. وهي تشير إلى عدد المنافسين (اللاعبين في السوق) الموجودين في مساحة سوق معينة نسبة إلى حجمها أو قيمتها السوقية الإجمالية.
الشركات الرئيسية العاملة في سوق الملفات الرئيسية للمحاكمة الإلكترونية (eTMF) هي:
- شركة أوريا
- تام شفاف
- شركة كوفانس (شركة مختبرية)
- أوراكل
- إينوف
إخلاء المسؤولية : الشركات المذكورة أعلاه ليست مرتبة بأي ترتيب معين.
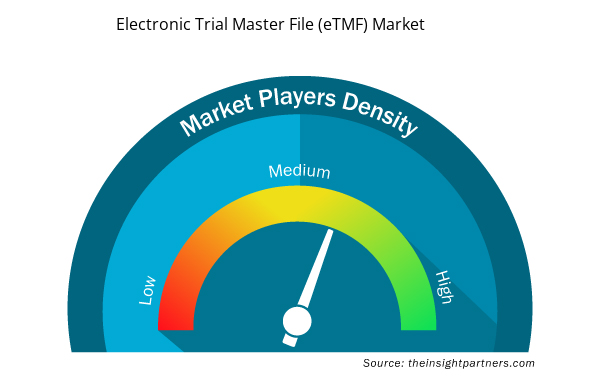
- احصل على نظرة عامة على أهم اللاعبين الرئيسيين في سوق الملفات الرئيسية للمحاكمة الإلكترونية (eTMF)
ملف المحاكمة الإلكتروني الرئيسي في سوق الرعاية الصحية – حسب المكون
- خدمة
- برمجة
ملف المحاكمة الإلكتروني الرئيسي في سوق الرعاية الصحية – حسب طريقة التسليم
- eTMF المستند إلى السحابة
- eTMF محليًا
ملف المحاكمة الإلكتروني الرئيسي في سوق الرعاية الصحية – حسب المستخدم النهائي
- شركات الأدوية والتكنولوجيا الحيوية
- منظمات العلاقات التعاقدية
- آحرون
ملف المحاكمة الإلكتروني في سوق الرعاية الصحية – حسب المنطقة الجغرافية
أمريكا الشمالية
- نحن
- كندا
- المكسيك
أوروبا
- فرنسا
- ألمانيا
- إيطاليا
- المملكة المتحدة
- إسبانيا
- بقية أوروبا
آسيا والمحيط الهادئ (APAC)
- الصين
- الهند
- كوريا الجنوبية
- اليابان
- أستراليا
- بقية منطقة آسيا والمحيط الهادئ
الشرق الأوسط وأفريقيا
- جنوب أفريقيا
- المملكة العربية السعودية
- الامارات العربية المتحدة
- باقي منطقة الشرق الأوسط وأفريقيا
أمريكا الجنوبية وأمريكا الوسطى (SCAM)
- البرازيل
- الأرجنتين
- بقية الاحتيال
نبذة عن الشركة
- شركة أوريا
- مثالي.
- شركة كوفانس (شركة مختبرية)
- أوراكل
- إينوف
- ماستر كنترول، المحدودة
- أومنيكوم
- اليقظة الدوائية
- أنظمة فييفا
- فليكس جلوبال
- التحليل التاريخي (سنتان)، السنة الأساسية، التوقعات (7 سنوات) مع معدل النمو السنوي المركب
- تحليل PEST و SWOT
- حجم السوق والقيمة / الحجم - عالميًا وإقليميًا وقطريًا
- الصناعة والمنافسة
- مجموعة بيانات Excel
- Electronic Signature Software Market
- Photo Editing Software Market
- Quantitative Structure-Activity Relationship (QSAR) Market
- Medical and Research Grade Collagen Market
- Glycomics Market
- Dried Blueberry Market
- Third Party Logistics Market
- Water Pipeline Leak Detection System Market
- Virtual Production Market
- Workwear Market

Report Coverage
Revenue forecast, Company Analysis, Industry landscape, Growth factors, and Trends
Segment Covered
This text is related
to segments covered.

Regional Scope
North America, Europe, Asia Pacific, Middle East & Africa, South & Central America
Country Scope
This text is related
to country scope.
الأسئلة الشائعة
Pharmaceutical and biotechnology companies, contract research organizations (CROs) and other users can make use of electronic trial master file (eTMF).
Increasing in number of clinical trial, increasing prevalence of diseases and technology advancement have been boosting the market over the years. However, dearth of skilled professionals is likely to have a negative impact on the growth of the market in the coming years. On the other hand, increasing strategic initiatives by market players is likely to provide growth opportunities over the coming years.
Electronic trial master file (eTMF) systems can be defined as an integration of software and hardware components collectively responsible for the optimal management of clinical trial data. These solutions help to streamline the data generated during the course of a clinical trial in an easy-to-store digital format, which can be retrieved by dissimilar users beneficial in easy accessibility and reduction the cost associated with the administrative and manual data maintenance operations in clinical trials.
Trends and growth analysis reports related to Technology, Media and Telecommunications : READ MORE..
The List of Companies - Electronic Trial Master File (eTMF) Market
- Aurea, Inc.
- TRANSPERFECT
- Covance Inc (Lab Corp)
- Oracle
- Ennov
- Mastercontrol, Inc.
- Omnicomm
- Pharmavigilalnce
- Veeva Systems
- Phlexglobal
The Insight Partners performs research in 4 major stages: Data Collection & Secondary Research, Primary Research, Data Analysis and Data Triangulation & Final Review.
- Data Collection and Secondary Research:
As a market research and consulting firm operating from a decade, we have published and advised several client across the globe. First step for any study will start with an assessment of currently available data and insights from existing reports. Further, historical and current market information is collected from Investor Presentations, Annual Reports, SEC Filings, etc., and other information related to company’s performance and market positioning are gathered from Paid Databases (Factiva, Hoovers, and Reuters) and various other publications available in public domain.
Several associations trade associates, technical forums, institutes, societies and organization are accessed to gain technical as well as market related insights through their publications such as research papers, blogs and press releases related to the studies are referred to get cues about the market. Further, white papers, journals, magazines, and other news articles published in last 3 years are scrutinized and analyzed to understand the current market trends.
- Primary Research:
The primarily interview analysis comprise of data obtained from industry participants interview and answers to survey questions gathered by in-house primary team.
For primary research, interviews are conducted with industry experts/CEOs/Marketing Managers/VPs/Subject Matter Experts from both demand and supply side to get a 360-degree view of the market. The primary team conducts several interviews based on the complexity of the markets to understand the various market trends and dynamics which makes research more credible and precise.
A typical research interview fulfils the following functions:
- Provides first-hand information on the market size, market trends, growth trends, competitive landscape, and outlook
- Validates and strengthens in-house secondary research findings
- Develops the analysis team’s expertise and market understanding
Primary research involves email interactions and telephone interviews for each market, category, segment, and sub-segment across geographies. The participants who typically take part in such a process include, but are not limited to:
- Industry participants: VPs, business development managers, market intelligence managers and national sales managers
- Outside experts: Valuation experts, research analysts and key opinion leaders specializing in the electronics and semiconductor industry.
Below is the breakup of our primary respondents by company, designation, and region:
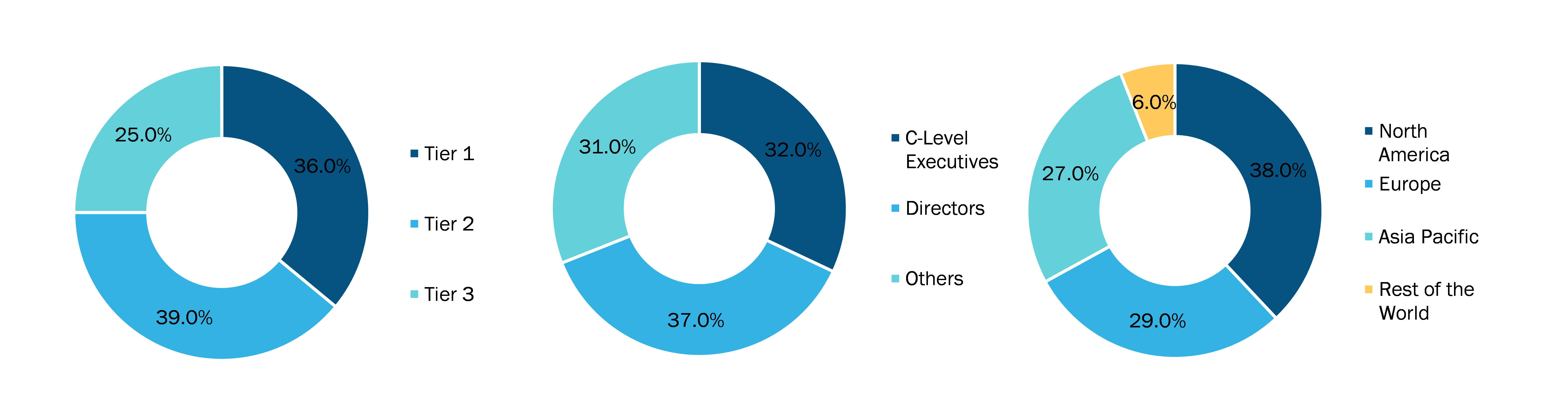
Once we receive the confirmation from primary research sources or primary respondents, we finalize the base year market estimation and forecast the data as per the macroeconomic and microeconomic factors assessed during data collection.
- Data Analysis:
Once data is validated through both secondary as well as primary respondents, we finalize the market estimations by hypothesis formulation and factor analysis at regional and country level.
- Macro-Economic Factor Analysis:
We analyse macroeconomic indicators such the gross domestic product (GDP), increase in the demand for goods and services across industries, technological advancement, regional economic growth, governmental policies, the influence of COVID-19, PEST analysis, and other aspects. This analysis aids in setting benchmarks for various nations/regions and approximating market splits. Additionally, the general trend of the aforementioned components aid in determining the market's development possibilities.
- Country Level Data:
Various factors that are especially aligned to the country are taken into account to determine the market size for a certain area and country, including the presence of vendors, such as headquarters and offices, the country's GDP, demand patterns, and industry growth. To comprehend the market dynamics for the nation, a number of growth variables, inhibitors, application areas, and current market trends are researched. The aforementioned elements aid in determining the country's overall market's growth potential.
- Company Profile:
The “Table of Contents” is formulated by listing and analyzing more than 25 - 30 companies operating in the market ecosystem across geographies. However, we profile only 10 companies as a standard practice in our syndicate reports. These 10 companies comprise leading, emerging, and regional players. Nonetheless, our analysis is not restricted to the 10 listed companies, we also analyze other companies present in the market to develop a holistic view and understand the prevailing trends. The “Company Profiles” section in the report covers key facts, business description, products & services, financial information, SWOT analysis, and key developments. The financial information presented is extracted from the annual reports and official documents of the publicly listed companies. Upon collecting the information for the sections of respective companies, we verify them via various primary sources and then compile the data in respective company profiles. The company level information helps us in deriving the base number as well as in forecasting the market size.
- Developing Base Number:
Aggregation of sales statistics (2020-2022) and macro-economic factor, and other secondary and primary research insights are utilized to arrive at base number and related market shares for 2022. The data gaps are identified in this step and relevant market data is analyzed, collected from paid primary interviews or databases. On finalizing the base year market size, forecasts are developed on the basis of macro-economic, industry and market growth factors and company level analysis.
- Data Triangulation and Final Review:
The market findings and base year market size calculations are validated from supply as well as demand side. Demand side validations are based on macro-economic factor analysis and benchmarks for respective regions and countries. In case of supply side validations, revenues of major companies are estimated (in case not available) based on industry benchmark, approximate number of employees, product portfolio, and primary interviews revenues are gathered. Further revenue from target product/service segment is assessed to avoid overshooting of market statistics. In case of heavy deviations between supply and demand side values, all thes steps are repeated to achieve synchronization.
We follow an iterative model, wherein we share our research findings with Subject Matter Experts (SME’s) and Key Opinion Leaders (KOLs) until consensus view of the market is not formulated – this model negates any drastic deviation in the opinions of experts. Only validated and universally acceptable research findings are quoted in our reports.
We have important check points that we use to validate our research findings – which we call – data triangulation, where we validate the information, we generate from secondary sources with primary interviews and then we re-validate with our internal data bases and Subject matter experts. This comprehensive model enables us to deliver high quality, reliable data in shortest possible time.

 احصل على عينة مجانية لهذا التقرير
احصل على عينة مجانية لهذا التقرير