من المتوقع أن يصل حجم سوق برامج مراقبة الأجهزة الطبية في أوروبا إلى 280.23 مليون دولار أمريكي بحلول عام 2031 من 143.9 مليون دولار أمريكي في عام 2023. ومن المتوقع أن يسجل السوق معدل نمو سنوي مركب بنسبة 8.7٪ خلال الفترة 2023-2031. ومن المرجح أن يجلب البرنامج كجهاز طبي مجموعة جديدة من الاتجاهات الرئيسية في السوق في السنوات القادمة.
تحليل سوق برامج مراقبة الأجهزة الطبية في أوروبا
إن زيادة الامتثال التنظيمي، وارتفاع التكنولوجيا الطبية، وزيادة تعقيد الأجهزة الطبية هي العوامل التي تدفع سوق برامج مراقبة الأجهزة الطبية في أوروبا . والهدف الرئيسي لنظام مراقبة الأجهزة الطبية هو تحسين حماية صحة وسلامة المرضى ومقدمي الرعاية الصحية والجمهور من خلال تقليل احتمالية تكرار الحوادث الضارة التي تنطوي على الأجهزة الطبية. ويتم تحقيق ذلك من خلال مجموعة متنوعة من الآليات. وتتضمن مراقبة الأجهزة الطبية جمع المعلومات الجديدة حول المخاطر المرتبطة باستخدام الأجهزة الطبية وتقييمها وفهمها والاستجابة لها. وتتمثل هذه المخاطر بشكل خاص في الحوادث الضارة والتفاعلات مع مواد أو أجهزة أخرى وموانع الاستعمال والتزوير والأعطال والعيوب الفنية.
نظرة عامة على سوق برامج مراقبة الأجهزة الطبية في أوروبا
الغرض الأساسي من برامج مراقبة الأجهزة الطبية هو دعم مراقبة الأجهزة الطبية بعد طرحها في السوق، وضمان استمرار سلامتها وفعاليتها طوال دورة حياتها. تعد مراقبة ما بعد التسويق أمرًا بالغ الأهمية لضمان عدم وجود أي أحداث سلبية أو مشاكل أخرى مع المنتج. يتم تحديد المخاطر المرتبطة بأي آثار غير متوقعة للاستخدام طويل الأمد ومعالجتها في أقرب وقت ممكن. الهدف من مراقبة ما بعد التسويق هو ضمان بقاء المنتجات آمنة وفعالة مع مراقبة فوائدها ومخاطرها باستمرار.
تتضمن ميزات برنامج مراقبة الأجهزة الطبية تقارير الحوادث المتعلقة بالأعطال، وجمع جميع البيانات ذات الصلة وفقًا لتقارير الأجهزة الطبية، وتعيين أرقام تقارير خاصة بالشركة المصنعة، واستيفاء جميع متطلبات الأعمال الورقية وحفظ السجلات؛ وتخزين بيانات الحوادث، وتحليل نسب الجهاز، وتقييم التقارير والتحقيق فيها لاسترجاع البيانات بسرعة وسهولة؛ وإنشاء العديد من التقارير لتقديمها إلى هيئات تنظيمية مختلفة في جميع أنحاء المنطقة.
تخصيص البحث ليناسب متطلباتك
يمكننا تحسين وتخصيص التحليل والنطاق الذي لم يتم تحقيقه من خلال عروضنا القياسية. ستساعدك هذه المرونة في الحصول على المعلومات الدقيقة اللازمة لتخطيط أعمالك واتخاذ القرارات.
سوق برامج مراقبة الأجهزة الطبية في أوروبا:
معدل النمو السنوي المركب (2023 - 2031)8.7%- حجم السوق بحلول عام 2023
143.9 مليون دولار أمريكي - حجم السوق 2031
280.23 مليون دولار أمريكي

ديناميكيات السوق
- "المتطلبات التنظيمية الصارمة المتعلقة بالأجهزة الطبية
- ارتفاع في التكنولوجيا الطبية
- "التعقيد المتزايد للأجهزة الطبية"
- البرمجيات كجهاز طبي
- التحول الرقمي في الرعاية الصحية
- نمو سوق الأجهزة الطبية
اللاعبون الرئيسيون
- شركة أوراكل
- مكعب AB SAS
- شركة سارجين سيستمز المحدودة
- شركة أشوركس
- شركة UL للحلول
- شركة هونيويل الدولية
- شركة بي تي سي
- شركة إنتل
- الحد الأقصى للتطبيق
- شركة زيبيون الرقمية
نظرة عامة إقليمية
- أوروبا
تقسيم السوق
 طلب
طلب- التشخيص
- علاجي
- جراحي
- بحث
 وضع النشر
وضع النشر- سحاب
- في الموقع
 الاستخدام النهائي العمودي
الاستخدام النهائي العمودي- منظمات البحوث السريرية
- الاستعانة بمصادر خارجية لعمليات الأعمال
- الشركات المصنعة للمعدات الأصلية
- يُظهر ملف PDF النموذجي بنية المحتوى وطبيعة المعلومات مع التحليل النوعي والكمي.
محركات وفرص سوق برامج مراقبة الأجهزة الطبية في أوروبا
زيادة تعقيد الأجهزة الطبية
تُعَد برامج الأجهزة الطبية مكونًا أساسيًا لأنظمة الرعاية الصحية الحديثة. وتُعَد الحلول البرمجية في سوق الأجهزة الطبية مطلوبة لإدارة واجهات المستخدم وبيانات المرضى واللوائح وتعقيد المنتج. ويقلل تبنيها من المخاطر أثناء تطوير الأجهزة الطبية وبرامجها ويساعد في تسريع تطوير البرامج ونشرها. كما تشرف على إدارة المخاطر في مجال الرعاية الصحية. ومع توسع سوق الأجهزة الطبية، يزداد تحدي تحقيق التوازن بين الأجهزة والبرامج واللوائح. ترتبط أدوات إدارة المتطلبات وبرامج مراقبة الأجهزة الطبية ارتباطًا وثيقًا في صناعة الرعاية الصحية فيما يتعلق بتطوير الأجهزة الطبية وإدارة دورة حياتها. وبالتالي، للتعامل مع تعقيد الأجهزة الطبية، يتزايد الطلب على برامج مراقبة الأجهزة الطبية.
لقد أدى التقدم في التقنيات الطبية إلى تحسين التشخيص والعلاجات من أجل تشخيصات مبكرة وأكثر دقة، وعلاجات أكثر فعالية، وضمان سلامة المرضى. تتطور الأجهزة الطبية بسرعة مع دمج النظام الرقمي، وتصميمات الأجهزة الطبية الحديثة والمدمجة، والاعتماد على نظام البرمجيات. وهذا يولد تعقيدًا من حيث المراقبة والإبلاغ وضمان سلامة الأجهزة الطبية. بالإضافة إلى ذلك، فإن الالتزام بالامتثال التنظيمي الأكثر صرامة يشجع مصنعي الأجهزة الطبية على تبني حلول برمجية متقدمة يمكنها التعامل مع التحديات الناجمة عن التعقيد المتزايد للأجهزة الطبية.
التحول الرقمي في الرعاية الصحية
يعمل قطاع الرعاية الصحية الرقمية في أوروبا على تعزيز استخدام مختلف التقنيات الرقمية التي تعمل على تحسين مرافق الرعاية الصحية. إن استخدام التقنيات الرقمية للمعلومات والاتصالات لإدارة المرض وتجنب المخاطر الصحية وتعزيز سلامة المرضى يدفع التحول الرقمي في قطاع الرعاية الصحية في أوروبا. تركز السلطات في أوروبا باستمرار على تقديم خدمات محسنة للمواطنين. ولهذا، فهي تشارك باستمرار في أنشطة الاستثمار. على سبيل المثال، تم اعتماد برنامج EU4Health بميزانية تزيد عن 5.9 مليار دولار أمريكي (5.3 مليار يورو) خلال الفترة 2021-2027 لبناء أنظمة صحية أقوى وأكثر مرونة وأكثر سهولة في الوصول إليها. يعزز هذا الاستثمار رقمنة نظام الرعاية الصحية والوصول إلى المنتجات الطبية والأجهزة الطبية والمنتجات ذات الصلة بالأزمات. مع غالبية المشاريع الجديدة الجارية بالفعل منذ ديسمبر 2023، فإن هدف المنح هو مساعدة دول الاتحاد الأوروبي على تنفيذ مساحة البيانات الصحية الأوروبية المستقبلية (EHDS). يمكن لمثل هذا الاستثمار أن يعزز الابتكار والتطوير وتبني برامج مراقبة الأجهزة الطبية التي تلبي المعايير التنظيمية وتحسن سلامة المرضى. إن اعتماد برامج اليقظة من شأنه أن يعزز مرونة الأنظمة الصحية أثناء الأزمات الصحية مثل كوفيد-19. ويمكنه تقديم تقارير أسرع وتحليل البيانات حول أداء الأجهزة الطبية. وخلال حالات الطوارئ، يمكنه دعم اتخاذ القرارات وإدارة المخاطر بشكل أسرع. وبالتالي، فإن رقمنة نظام الرعاية الصحية في أوروبا تدفع إلى تحقيق تقدم كبير في جميع جوانب الرعاية الصحية، مما يخلق الإمكانات للصناعة لتقديم نتائج صحية أفضل بكفاءة أكبر. يتيح هذا العامل اعتماد حلول لتقليل المخاطر على الجودة ويزيد من الوقت اللازم لطرح المنتجات في السوق والامتثال التنظيمي، مما يعزز الطلب على برامج اليقظة للأجهزة الطبية في أوروبا.
تقرير تحليلي لتجزئة سوق برامج مراقبة الأجهزة الطبية في أوروبا
كانت القطاعات الرئيسية التي ساهمت في اشتقاق تحليل سوق برامج مراقبة الأجهزة الطبية في أوروبا هي التطبيق، ووضع النشر، والاستخدام النهائي.
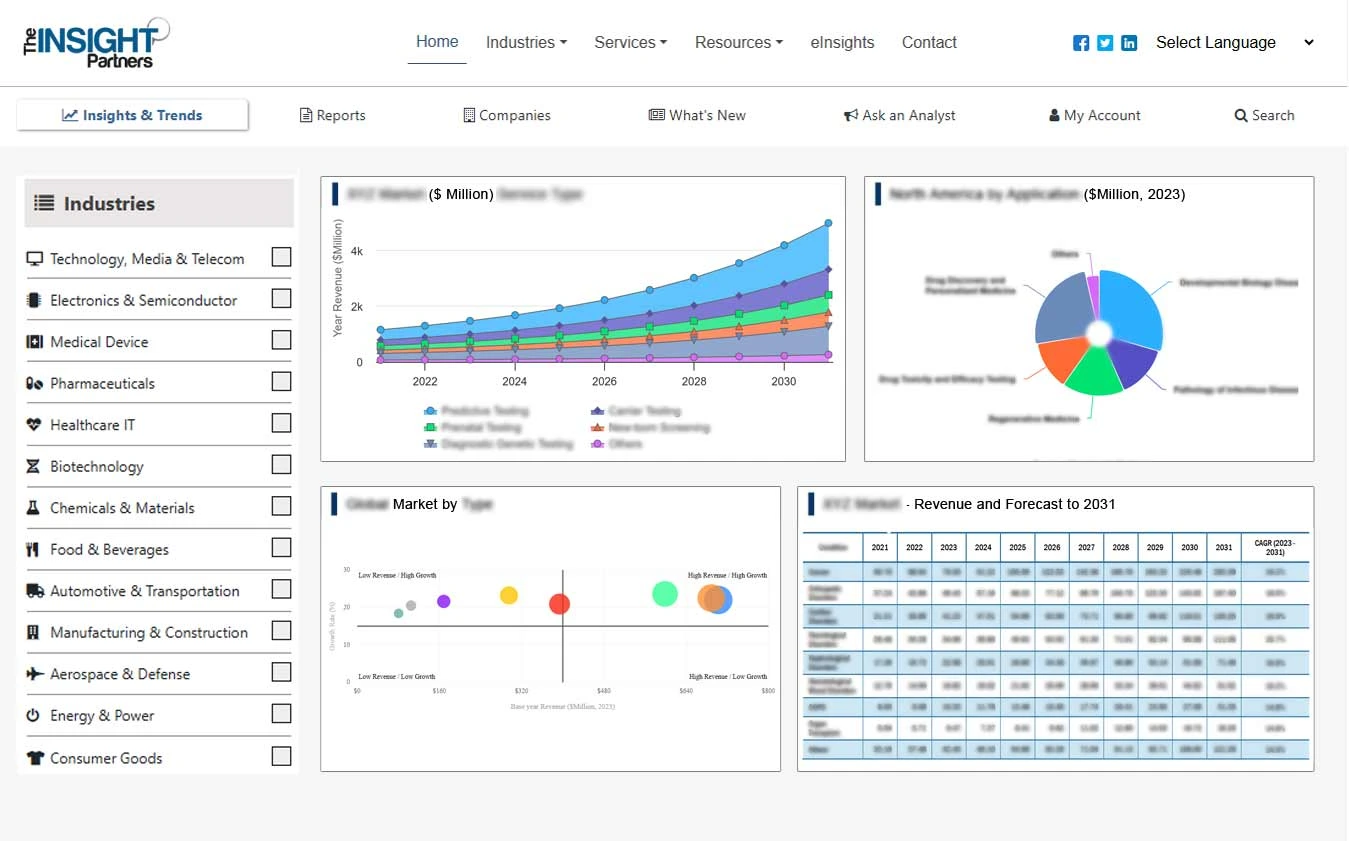
- بناءً على التطبيق، ينقسم السوق إلى التشخيص والعلاج والجراحة والبحث وغيرها. احتل قطاع التشخيص أكبر حصة في سوق برامج مراقبة الأجهزة الطبية في أوروبا في عام 2023.
- بناءً على وضع النشر، ينقسم السوق إلى سحابي ومحلي. احتل قطاع السحابة حصة أكبر في سوق برامج مراقبة الأجهزة الطبية في أوروبا في عام 2023.
- بناءً على الاستخدام النهائي، يتم تقسيم السوق إلى شركات البحث التعاقدي، وشركات الاستعانة بمصادر خارجية، وشركات تصنيع المعدات الأصلية، وغيرها. احتلت شريحة الشركات المصنعة للمعدات الأصلية (OEMs) أكبر حصة في سوق برامج مراقبة الأجهزة الطبية في أوروبا في عام 2023.
تحليل حصة سوق برامج مراقبة الأجهزة الطبية في أوروبا حسب المنطقة الجغرافية
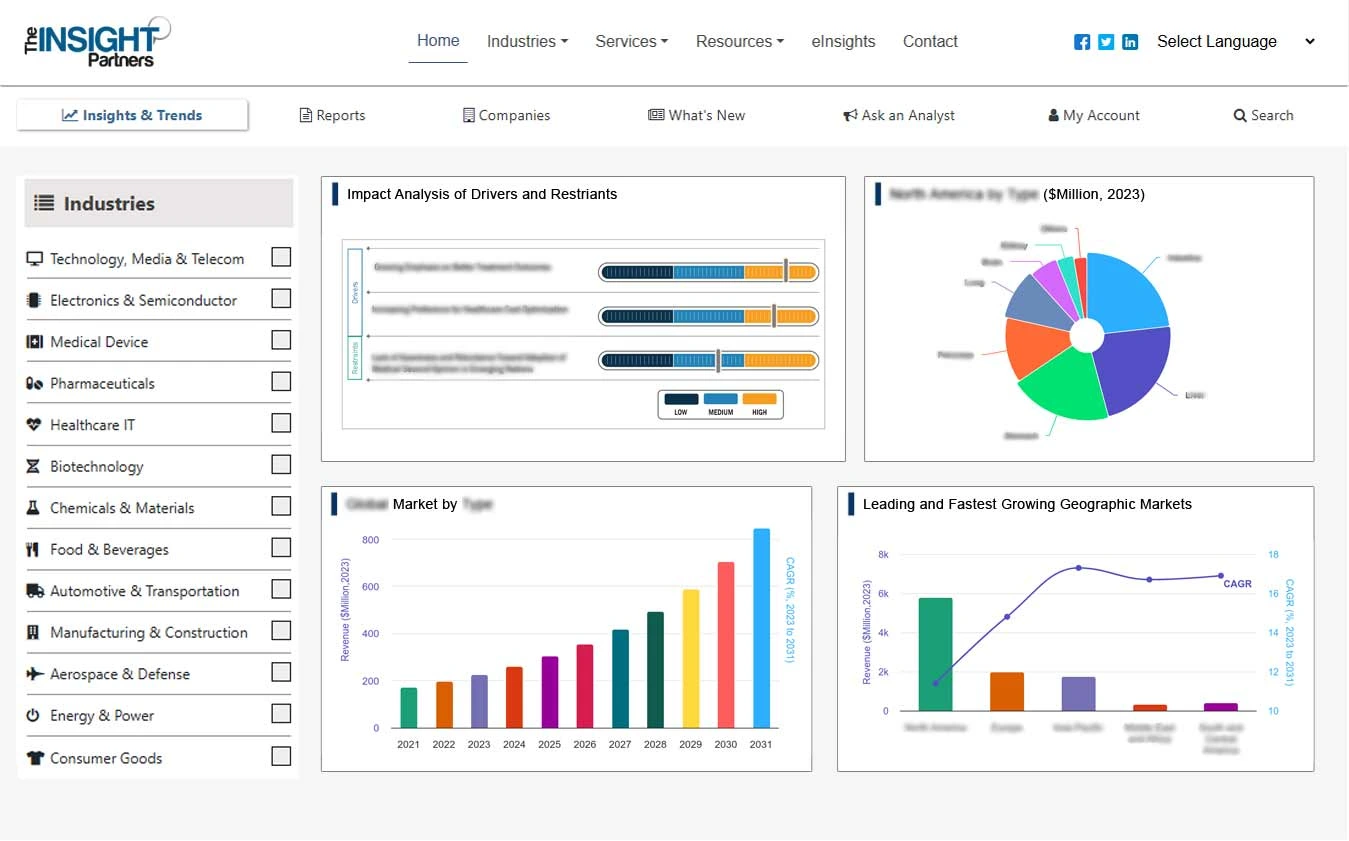
تم تقسيم سوق برامج مراقبة الأجهزة الطبية في أوروبا إلى ألمانيا وفرنسا والمملكة المتحدة وروسيا وإسبانيا وبقية أوروبا. سيطرت ألمانيا على السوق في عام 2023، تليها فرنسا والمملكة المتحدة.
يجب الإبلاغ عن الحوادث الضارة التي تنطوي على الأجهزة الطبية في المملكة المتحدة إلى وكالة تنظيم الأدوية ومنتجات الرعاية الصحية (MHRA). تشرف MHRA على سوق الأجهزة الطبية في المملكة المتحدة. بمجرد طرح جهاز طبي في سوق المملكة المتحدة، يلتزم المصنع بتقديم تقارير اليقظة إلى MHRA كلما حدثت أنواع معينة من الحوادث التي تنطوي على أجهزتهم في المملكة المتحدة. يجب على المصنع أيضًا اتخاذ تدابير السلامة المناسبة عند الضرورة. يجب على المصنع التأكد من أن أجهزته تلبي معايير السلامة والأداء المعمول بها طوال مدة استخدامها. يجب على مصنع الجهاز الطبي أو الشخص المسؤول في المملكة المتحدة أو الممثل المعتمد الموجود في أيرلندا الشمالية الإبلاغ إلى MHRA عن الحوادث المتعلقة بالأجهزة الطبية وتقارير اليقظة بعد التسويق. تعمل مثل هذه التفويضات لتقرير نظام اليقظة والمراقبة على دفع الطلب على برامج اليقظة للأجهزة الطبية للإبلاغ الفعال والمراقبة بعد التسويق.
نطاق تقرير سوق برامج مراقبة الأجهزة الطبية في أوروبا
| سمة التقرير | تفاصيل |
|---|---|
| حجم السوق في عام 2023 | 143.9 مليون دولار أمريكي |
| حجم السوق بحلول عام 2031 | 280.23 مليون دولار أمريكي |
| معدل النمو السنوي المركب العالمي (2023 - 2031) | 8.7% |
| البيانات التاريخية | 2021-2022 |
| فترة التنبؤ | 2024-2031 |
| القطاعات المغطاة | حسب الطلب
|
| المناطق والدول المغطاة | أوروبا
|
| قادة السوق وملفات تعريف الشركات الرئيسية |
|
- يُظهر ملف PDF النموذجي بنية المحتوى وطبيعة المعلومات مع التحليل النوعي والكمي.
أخبار السوق الأوروبية لبرامج مراقبة الأجهزة الطبية والتطورات الأخيرة
يتم تقييم سوق برامج مراقبة الأجهزة الطبية في أوروبا من خلال جمع البيانات النوعية والكمية بعد البحث الأولي والثانوي، والذي يتضمن منشورات الشركات المهمة وبيانات الجمعيات وقواعد البيانات. فيما يلي بعض التطورات في سوق برامج مراقبة الأجهزة الطبية في أوروبا:
- أعلنت شركة أوراكل عن قدرات جديدة في حلول Oracle Argus وSafety One Intake المدعومة بالذكاء الاصطناعي لمساعدة مؤسسات العلوم الحيوية على تلبية المتطلبات التنظيمية المتطورة وحجم العمل المتزايد لحالات الأحداث الضارة. من خلال التحسينات الجديدة المصممة لزيادة الإنتاجية وتحسين خصوصية البيانات وتعزيز إعداد التقارير، يمكن للمستخدمين معالجة اللوائح والمتطلبات الديناميكية الخاصة بكل بلد بكفاءة أكبر وتسريع موثوقية وشفافية إدارة حالات السلامة من التجارب السريرية إلى المراقبة بعد التسويق. (المصدر: شركة أوراكل، بيان صحفي، يوليو 2024)
- كشفت شركة Ab Cube عن أربعة تطبيقات جديدة لليقظة من الجيل التالي للذكاء الاصطناعي في AB Cube Galaxy. توفر هذه الوحدات الجديدة تحسينات قوية لمجموعة SafetyEasy الأساسية لعمليات اليقظة المتعددة السريعة والفعالة والقابلة للتطوير. تطبق الوحدة الجديدة التي تعمل بالذكاء الاصطناعي للشركة تقنية معالجة اللغة الطبيعية المتقدمة (NLP)، مما يسمح للعملاء بنسخ ولصق نص ICSR الخاص بهم، والذي يتم تحويله تلقائيًا إلى حالة في SafetyEasy Suite - مما يقلل من جهد قبول الحالات بنسبة 70٪. (المصدر: شركة Ab Cube، بيان صحفي، يونيو 2024)
تقرير سوق برامج مراقبة الأجهزة الطبية في أوروبا والتغطية والنتائج المتوقعة
يوفر "حجم سوق برامج مراقبة الأجهزة الطبية في أوروبا وتوقعاتها (2021-2031)" تحليلاً مفصلاً للسوق يغطي المجالات المذكورة أدناه:
- حجم سوق برامج مراقبة الأجهزة الطبية في أوروبا وتوقعاتها على المستوى الإقليمي والوطني لجميع قطاعات السوق الرئيسية المغطاة ضمن النطاق
- اتجاهات سوق برامج مراقبة الأجهزة الطبية في أوروبا ، بالإضافة إلى ديناميكيات السوق مثل المحركات والقيود والفرص الرئيسية
- تحليل مفصل لـ PEST و SWOT
- تحليل سوق برامج مراقبة الأجهزة الطبية في أوروبا يغطي اتجاهات السوق الرئيسية والإطار الإقليمي واللاعبين الرئيسيين واللوائح والتطورات الأخيرة في السوق
- تحليل المشهد الصناعي والمنافسة الذي يغطي تركيز السوق، وتحليل خريطة الحرارة، واللاعبين البارزين، والتطورات الأخيرة لسوق برامج مراقبة الأجهزة الطبية في أوروبا
- ملفات تعريف الشركة التفصيلية
- التحليل التاريخي (سنتان)، السنة الأساسية، التوقعات (7 سنوات) مع معدل النمو السنوي المركب
- تحليل PEST و SWOT
- حجم السوق والقيمة / الحجم - عالميًا وإقليميًا وقطريًا
- الصناعة والمنافسة
- مجموعة بيانات Excel
- Vision Guided Robotics Software Market
- Aerosol Paints Market
- Artificial Intelligence in Defense Market
- Vertical Farming Crops Market
- Long Read Sequencing Market
- Hair Wig Market
- Single-Use Negative Pressure Wound Therapy Devices Market
- Transdermal Drug Delivery System Market
- Rugged Phones Market
- Hydrogen Compressors Market

Report Coverage
Revenue forecast, Company Analysis, Industry landscape, Growth factors, and Trends
Segment Covered
This text is related
to segments covered.

Regional Scope
North America, Europe, Asia Pacific, Middle East & Africa, South & Central America
Country Scope
This text is related
to country scope.
الأسئلة الشائعة
The Europe medical device vigilance software market was estimated to be US$ 143.90 million in 2023 and is expected to grow at a CAGR of 8.7% during the forecast period 2024 - 2031.
Stringent regulatory requirements related to medical devices, rise in medical technology, and increased complexity of medical devices are the major factors that propel the Europe medical device vigilance software market.
Software as a Medical Device is anticipated to play a significant role in the Europe medical device vigilance software market in the coming years.
The key players holding majority shares in the Europe medical device vigilance software market are AB Cube S.A.S.; AssurX, Inc.; Oracle Corporation; Sparta Systems (Honeywell International Inc.); and Sarjen Systems Pvt. Ltd.
The Europe medical device vigilance software market is expected to reach US$ 280.23 million by 2031.
The incremental growth expected to be recorded for the Europe medical device vigilance software market during the forecast period is US$ 136.33 million.
Trends and growth analysis reports related to Technology, Media and Telecommunications : READ MORE..
The List of Companies - Europe Medical Device Vigilance Software Market
- Oracle Corp
- AB Cube S.A.S.
- Sarjen Systems Pvt. Ltd
- AssurX, Inc.
- UL Solutions Inc
- Honeywell International Inc
- PTC Inc
- Intel Corp
- Max Application
- Xybion Digital Inc.
The Insight Partners performs research in 4 major stages: Data Collection & Secondary Research, Primary Research, Data Analysis and Data Triangulation & Final Review.
- Data Collection and Secondary Research:
As a market research and consulting firm operating from a decade, we have published and advised several client across the globe. First step for any study will start with an assessment of currently available data and insights from existing reports. Further, historical and current market information is collected from Investor Presentations, Annual Reports, SEC Filings, etc., and other information related to company’s performance and market positioning are gathered from Paid Databases (Factiva, Hoovers, and Reuters) and various other publications available in public domain.
Several associations trade associates, technical forums, institutes, societies and organization are accessed to gain technical as well as market related insights through their publications such as research papers, blogs and press releases related to the studies are referred to get cues about the market. Further, white papers, journals, magazines, and other news articles published in last 3 years are scrutinized and analyzed to understand the current market trends.
- Primary Research:
The primarily interview analysis comprise of data obtained from industry participants interview and answers to survey questions gathered by in-house primary team.
For primary research, interviews are conducted with industry experts/CEOs/Marketing Managers/VPs/Subject Matter Experts from both demand and supply side to get a 360-degree view of the market. The primary team conducts several interviews based on the complexity of the markets to understand the various market trends and dynamics which makes research more credible and precise.
A typical research interview fulfils the following functions:
- Provides first-hand information on the market size, market trends, growth trends, competitive landscape, and outlook
- Validates and strengthens in-house secondary research findings
- Develops the analysis team’s expertise and market understanding
Primary research involves email interactions and telephone interviews for each market, category, segment, and sub-segment across geographies. The participants who typically take part in such a process include, but are not limited to:
- Industry participants: VPs, business development managers, market intelligence managers and national sales managers
- Outside experts: Valuation experts, research analysts and key opinion leaders specializing in the electronics and semiconductor industry.
Below is the breakup of our primary respondents by company, designation, and region:
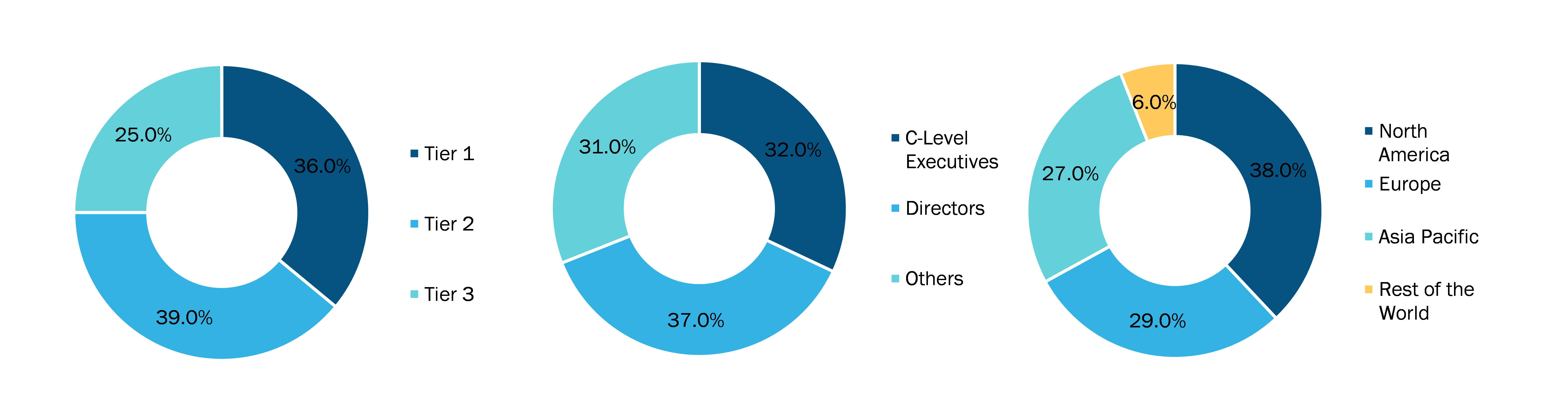
Once we receive the confirmation from primary research sources or primary respondents, we finalize the base year market estimation and forecast the data as per the macroeconomic and microeconomic factors assessed during data collection.
- Data Analysis:
Once data is validated through both secondary as well as primary respondents, we finalize the market estimations by hypothesis formulation and factor analysis at regional and country level.
- Macro-Economic Factor Analysis:
We analyse macroeconomic indicators such the gross domestic product (GDP), increase in the demand for goods and services across industries, technological advancement, regional economic growth, governmental policies, the influence of COVID-19, PEST analysis, and other aspects. This analysis aids in setting benchmarks for various nations/regions and approximating market splits. Additionally, the general trend of the aforementioned components aid in determining the market's development possibilities.
- Country Level Data:
Various factors that are especially aligned to the country are taken into account to determine the market size for a certain area and country, including the presence of vendors, such as headquarters and offices, the country's GDP, demand patterns, and industry growth. To comprehend the market dynamics for the nation, a number of growth variables, inhibitors, application areas, and current market trends are researched. The aforementioned elements aid in determining the country's overall market's growth potential.
- Company Profile:
The “Table of Contents” is formulated by listing and analyzing more than 25 - 30 companies operating in the market ecosystem across geographies. However, we profile only 10 companies as a standard practice in our syndicate reports. These 10 companies comprise leading, emerging, and regional players. Nonetheless, our analysis is not restricted to the 10 listed companies, we also analyze other companies present in the market to develop a holistic view and understand the prevailing trends. The “Company Profiles” section in the report covers key facts, business description, products & services, financial information, SWOT analysis, and key developments. The financial information presented is extracted from the annual reports and official documents of the publicly listed companies. Upon collecting the information for the sections of respective companies, we verify them via various primary sources and then compile the data in respective company profiles. The company level information helps us in deriving the base number as well as in forecasting the market size.
- Developing Base Number:
Aggregation of sales statistics (2020-2022) and macro-economic factor, and other secondary and primary research insights are utilized to arrive at base number and related market shares for 2022. The data gaps are identified in this step and relevant market data is analyzed, collected from paid primary interviews or databases. On finalizing the base year market size, forecasts are developed on the basis of macro-economic, industry and market growth factors and company level analysis.
- Data Triangulation and Final Review:
The market findings and base year market size calculations are validated from supply as well as demand side. Demand side validations are based on macro-economic factor analysis and benchmarks for respective regions and countries. In case of supply side validations, revenues of major companies are estimated (in case not available) based on industry benchmark, approximate number of employees, product portfolio, and primary interviews revenues are gathered. Further revenue from target product/service segment is assessed to avoid overshooting of market statistics. In case of heavy deviations between supply and demand side values, all thes steps are repeated to achieve synchronization.
We follow an iterative model, wherein we share our research findings with Subject Matter Experts (SME’s) and Key Opinion Leaders (KOLs) until consensus view of the market is not formulated – this model negates any drastic deviation in the opinions of experts. Only validated and universally acceptable research findings are quoted in our reports.
We have important check points that we use to validate our research findings – which we call – data triangulation, where we validate the information, we generate from secondary sources with primary interviews and then we re-validate with our internal data bases and Subject matter experts. This comprehensive model enables us to deliver high quality, reliable data in shortest possible time.
 احصل على عينة مجانية لهذا التقرير
احصل على عينة مجانية لهذا التقرير