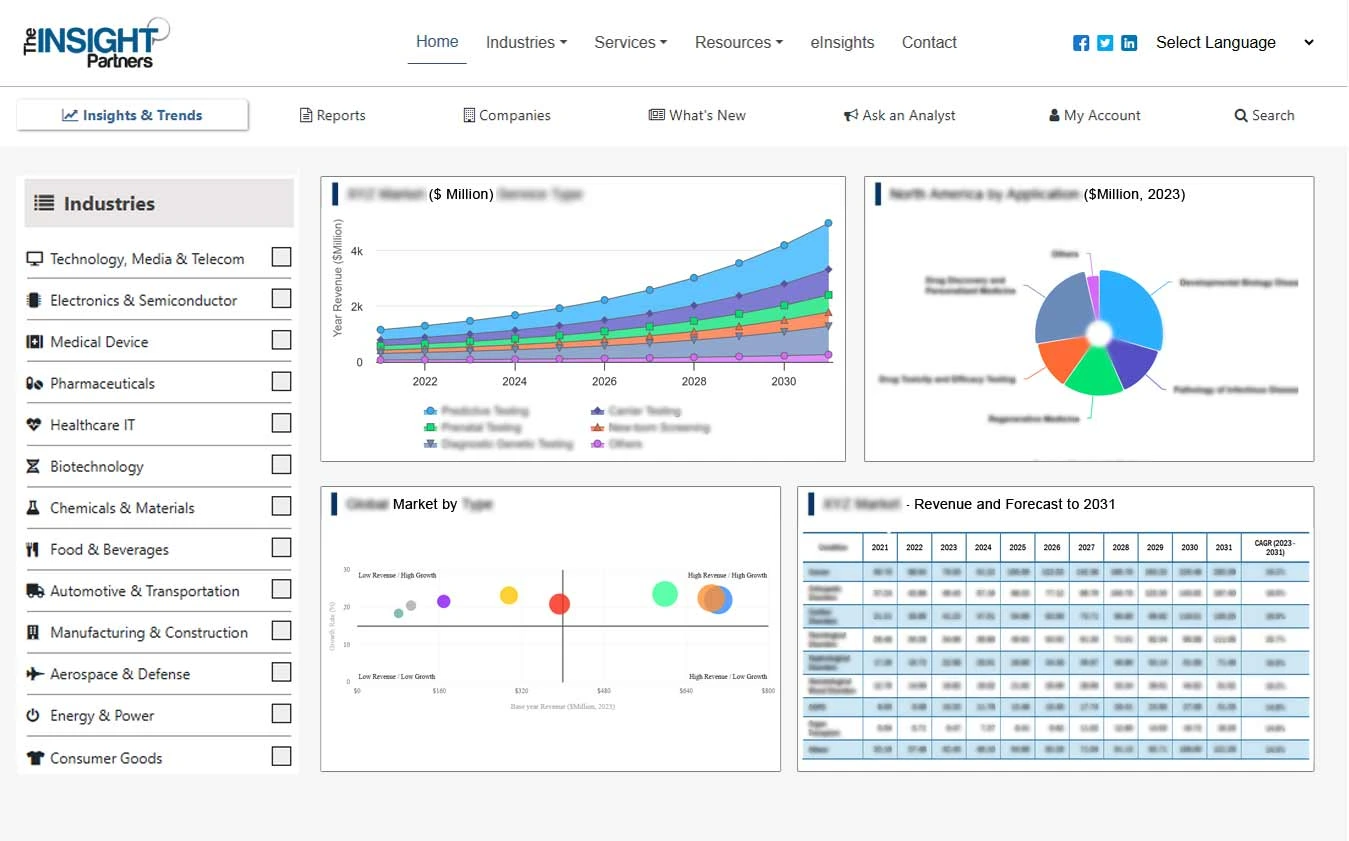
[Forschungsbericht] Die Größe des Marktes für Managementsysteme für klinische Studien wird voraussichtlich von 1410,98 Millionen US-Dollar im Jahr 2022 auf 2061,86 Millionen US-Dollar im Jahr 2030 wachsen; Es wird geschätzt, dass der Markt von 2022 bis 2030 eine jährliche Wachstumsrate von 12,56 % verzeichnen wird.
Sicht des Analysten
Die Marktanalyse für klinische Studienmanagementsysteme bringt Markttreiber mit sich, wie etwa die steigende Zahl neuartiger chronischer Krankheiten und Arzneimittelentwicklungsaktivitäten, die zu einer steigenden Zahl klinischer Studien geführt haben. Die zunehmende Zahl klinischer Studien steigert wiederum die Nachfrage nach Managementsystemen für klinische Studien. Es wird jedoch erwartet, dass die Budgetbeschränkung das Wachstum des Marktes im Prognosezeitraum behindern wird. Je nach Typ wird der Markt in Unternehmen und Vor-Ort-Markt unterteilt. Das Softwaresegment hatte im Jahr 2022 den größten Marktanteil. Darüber hinaus schafft die Integration von CTMS in bestehende Software Chancen auf dem Markt für Managementsysteme für klinische Studien im Zeitraum 2023–2030. Je nach Typ ist der Markt für Managementsysteme für klinische Studien in Unternehmen und Vor-Ort unterteilt. Das Unternehmenssegment hatte im Jahr 2022 den größten Marktanteil und wird voraussichtlich mit der höchsten CAGR wachsen.
Klinische Studien sind Experimente, die durchgeführt werden, um die Sicherheit und Wirksamkeit neuer Behandlungen sicherzustellen. Pharmazeutische, biotechnische oder medizinische Geräteunternehmen sponsern diese Studien, um die Genehmigung der FDA oder einer internationalen Regulierungsbehörde für ihr Medikament oder Gerät einzuholen. Das Clinical Trial Management System (CTMS) ist darauf ausgelegt, Informationen intuitiv zu verfolgen und logisch zu strukturieren. Dadurch können Life-Science-Teams den Fortschritt klinischer Studien überwachen und darüber Bericht erstatten, fundiertere Entscheidungen treffen und Daten von höchster Qualität bereitstellen und gleichzeitig die Patientensicherheit gewährleisten.
Strategische Einblicke
Markteinblicke
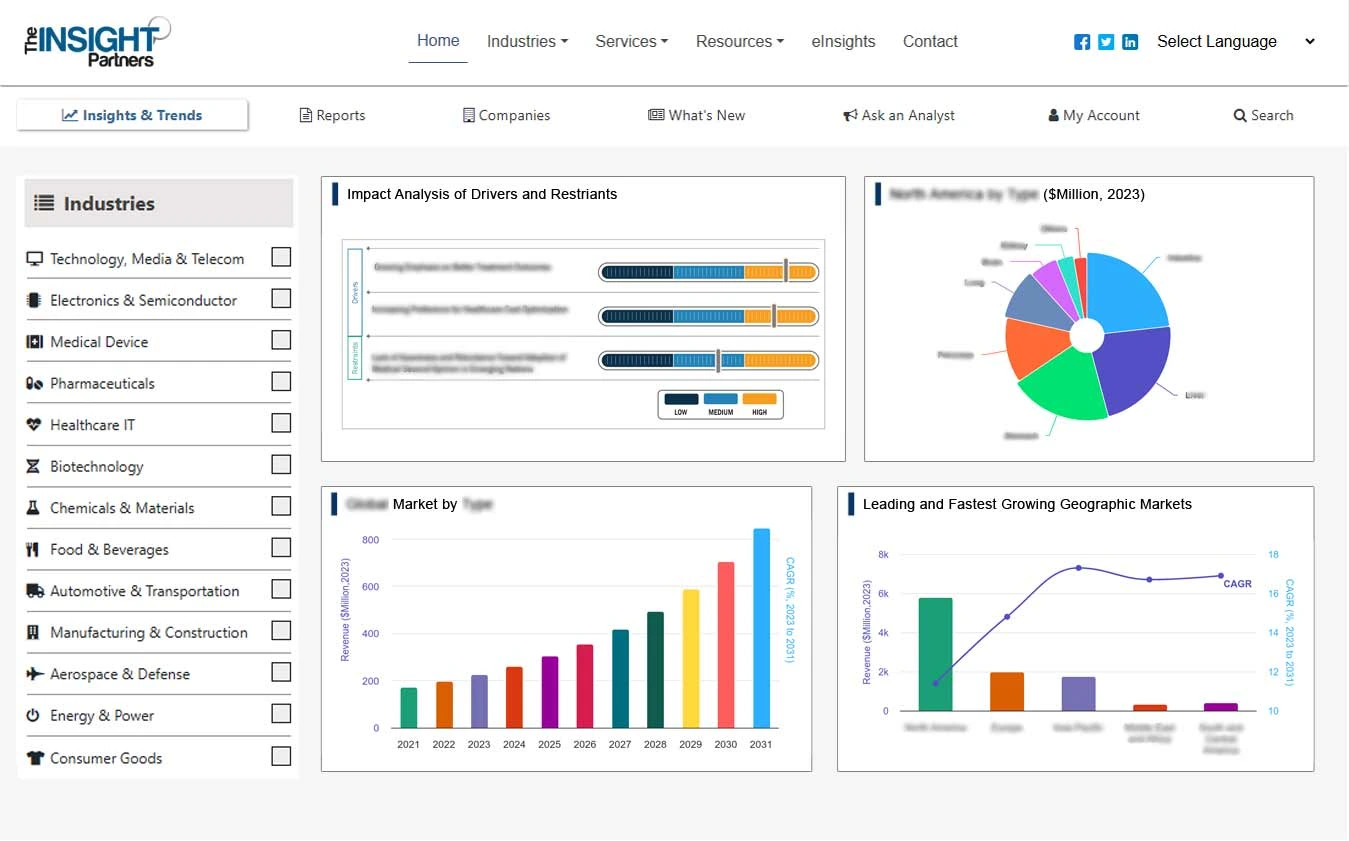
Steigende Zahl klinischer Studien treibt das Marktwachstum voran
Klinische Studien sind ein wichtiger Bestandteil der evidenzbasierten Medizin, weil sie helfen bei der Bestimmung der Wirkung neuer medizinischer Behandlungen, Diagnostika oder Impfstoffe. Sie beziehen häufig große Personengruppen ein, um sicherzustellen, dass die neue Intervention sicher und wirksam ist. Die Studien werden überwiegend im Rahmen der Arzneimittelentwicklung durchgeführt. Den Daten der National Library of Medicine (NLM) zufolge wurden im Jahr 2021 etwa 52.000 neue Studien bei NLM (ClinicalTrials.gov) registriert, ein Anstieg auf etwa 58.000 im Jahr 2023. Im Januar 2023 meldete die NLM 38.837 aktive klinische Studien in den USA und 105.172 aktive Studien weltweit. Nach Angaben der Europäischen Arzneimittel-Agentur werden in der Europäischen Union (EU) jährlich etwa 4.000 klinische Studien genehmigt, von denen etwa 60 % mit der Pharmaindustrie in Zusammenhang stehen. Eine zunehmende Zahl klinischer Studien zur Entwicklung verschiedener wirksamer Behandlungen aufgrund der weltweit steigenden Prävalenz chronischer Krankheiten treibt das Wachstum des Marktes für klinische Studien voran. Mit größeren Stichproben, diversifizierten Patientendemografien und mehreren Studienzentren werden klinische Studien immer komplexer. CTMS-Systeme tragen dazu bei, Versuchsabläufe zu rationalisieren, das Datenmanagement zu verbessern und die Zusammenarbeit der Beteiligten zu verbessern. Darüber hinaus erzeugen klinische Studien riesige Datenmengen, die sorgfältig gesammelt, verarbeitet und analysiert werden müssen. CTMS-Plattformen umfassen Datenintegration, Echtzeitberichte und Datenvisualisierungsfunktionen, die es Forschern und Sponsoren ermöglichen, fundierte Entscheidungen zu treffen und die Effizienz von Studien zu steigern. Darüber hinaus ist die Einhaltung regulatorischer Anforderungen im Pharmasektor, der stark reguliert ist, von entscheidender Bedeutung. CTMS-Systeme verbessern Compliance-Aktivitäten, indem sie Tools zur Verwaltung der regulatorischen Dokumentation, zur Gewährleistung der Protokolleinhaltung und zur Wahrung der Datenintegrität bereitstellen.
Darüber hinaus kurbelt die Einführung fortschrittlicher Innovationen durch Marktteilnehmer das Wachstum an des Marktes im Zeitraum 2022-2030. Beispielsweise stellte Oracle Corporation, ein führendes Technologieunternehmen, im Jahr 2023 seine neueste CTMS-Lösung namens Oracle Health Sciences Clinical One CTMS vor. Diese neue Lösung verfügt über erweiterte Funktionen wie Echtzeit-Datenanalyse, zentralisiertes Datenmanagement und verbesserte Compliance-Funktionen, die darauf abzielen, klinische Studienprozesse zu vereinfachen und die Gesamteffizienz zu steigern.
Chancen
Die Integration von CTMS in bestehende Systeme schafft Chancen für den CTMS-Markt
CTMS-Systeme, die sich nahtlos in EHR-Systeme integrieren lassen, können Patientendaten während klinischer Studien besser verwalten. Die Integration von Software für elektronische Patientenakten (EMR) in Software für klinische Studien wird als logischer nächster Schritt in der Datenverarbeitung angesehen, nachdem die Technologie der elektronischen Datenerfassung (EDC) das Papier ersetzt hat. Diese Integration würde eine genauere und effizientere Datenerfassung für klinische Studien ermöglichen, insbesondere bei Studien an mehreren Standorten. Laut einem im April 2023 von BMC veröffentlichten Artikel wurde eine Studie zur Entwicklung eines integrierten Systems zur Verwaltung klinischer Studien durchgeführt, um den Managementprozess klinischer Studien durch Systementwicklungsmethoden, Standardisierungsprotokolle, effiziente Integration mit externen Geschäftssystemen und Datensicherheit zu optimieren und Datenschutz. Eine effiziente Datenintegration wurde durch den Einsatz von Extract-Transform-Load-, Message-Queue- und Remote-Procedure-Call-Diensten erreicht, die das CTMS mit externen Systemen wie dem Hospital Information System (HIS), dem Laboratory Information System (LIS) und Electronic Medical verbanden Record (EMR) und Clinical Data Repository (CDR).
Im Oktober 2022 arbeitete RealTime Software Solutions, LLC mit Aspen Insights zusammen, um eine erstklassige EMR/EHR-Patientenidentifizierung zu integrieren Technologien in das erstklassige Clinical Trial Management System (CTMS) von RealTime integrieren. Die Integration des Unternehmens ermöglichte es klinischen Forschungsstandorten, strukturierte und unstrukturierte EMR/EHR-Daten für die Machbarkeitsanalyse von Studien, die Analyse der Eignung von Praxispopulationen, die Beurteilung von Ärzten und die direkte Bereitstellung vorqualifizierter Teilnehmer in RealTime-CTMS zu analysieren.
Berichtssegmentierung und -umfang
Typbasierte Erkenntnisse
Je nach Typ ist der Markt für Managementsysteme für klinische Studien in Unternehmens-CTMS und Vor-Ort-CTMS unterteilt. Das Unternehmenssegment hatte im Jahr 2022 den größten Marktanteil; Es wird erwartet, dass es zwischen 2022 und 2030 die höchste CAGR verzeichnen wird. Das Enterprise CTMS ist ein komplettes klinisches Forschungsmanagementsystem für mittlere bis große Organisationen mit hohen Anforderungen. Das Segment wächst aufgrund technologischer Fortschritte im Gesundheitssektor und zunehmender Produkteinführungen der führenden Marktteilnehmer im CTMS-Markt.
Im Oktober 2022 wurde Veeva Vault CTMS eingeführt von Veeva Systems wurde von 40 Auftragsforschungsorganisationen (CROs), darunter vier der sechs weltweit führenden CROs, ausgewählt, um schnellere und effizientere klinische Studien zu gewährleisten. Vault CTMS ist ein unternehmensweites Studienmanagementsystem, das von mehr als 120 Sponsoren ausgewählt wurde, darunter 9 der 20 größten Pharmaunternehmen.
Delivery-Based Insights
Basierend auf der Bereitstellung ist der Markt für Managementsysteme für klinische Studien in webgehostete, cloudbasierte und On-Premise-Systeme unterteilt. Das webgehostete Segment hielt im Jahr 2022 aufgrund seiner Vorteile, darunter eine verbesserte Qualität und Effizienz klinischer Studien, ein besseres Zeitmanagement und einen einfachen Zugang, den größten Marktanteil. Es wird erwartet, dass das Cloud-basierte Segment im Zeitraum 2022–2030 aufgrund der verschiedenen Produkteinführungen führender Marktteilnehmer die höchste CAGR verzeichnen wird. Im Dezember 2021 kündigte SureClinical, ein führender Anbieter cloudnativer eClinical-Anwendungen, die Einführung seines neuen Clinical Ecosystem (ECO) Applications and Platform Bundle an. Das ECO-Paket ist speziell auf die besonderen Bedürfnisse klinischer Forschungsorganisationen zugeschnitten. Es verbindet Menschen, Programme, Projekte und Prozesse flächendeckend und sorgt so für eine nahtlose Sicht auf klinische Daten. Das ECO Bundle zentralisiert klinische Informationen und Berichte über mehrere Anwendungen, Datenpunkte und Systeme hinweg und ermöglicht so verteilten klinischen Forschungsteams die Zusammenarbeit innerhalb einer einzigen, modernen und benutzerfreundlichen Anwendungserfahrung.
< p>Endbenutzerbasierte Erkenntnisse
In Bezug auf Endbenutzer Für Benutzer ist der Markt für Managementsysteme für klinische Studien in Pharma- und Biotechnologieunternehmen, Medizingeräteunternehmen, CROs und andere unterteilt. Das Segment der Pharma- und Biotechnologieunternehmen hielt im Jahr 2022 den größten Marktanteil, und das Segment der CROs wird voraussichtlich im Zeitraum 2022–2030 die höchste CAGR verzeichnen, da klinische Studien auf die CROs verlagert werden, da der Life-Science-Sektor aktiv beteiligt ist bei der Auslagerung der Arzneimittelentwicklung und klinischer Studien an CROs. CROs helfen bei der erfolgreichen Durchführung klinischer Studien durch die angebotenen Dienstleistungen, die auf hochwertigen Einrichtungen und fundiertem Fachwissen basieren. CROs fungieren durch ihre effizienten und kosteneffizienten Abläufe, von denen Studiensponsoren profitieren, mittlerweile als Rückgrat der Branche für klinische Studien. Laut dem auf Thermo Fisher Scientific veröffentlichten Blog wurden im Jahr 2022 etwa drei von vier klinischen Studien von Auftragsforschungsinstituten durchgeführt, um die klinischen Programme der Arzneimittelentwickler zu bestätigen, umfassendes Fachwissen bereitzustellen, Zeit- und Kosteneffizienz zu erzielen und maßgeschneiderte, hochwertige Daten. Daher treiben die Entwicklung kostengünstiger Lösungen und die Verringerung von Fehlern bei CROs während des Arzneimittelentwicklungsprozesses das Wachstum des Marktes für klinische Studien voran.
Clinical Trial Management System, von Geben Sie – 2022 und 2030
Regionale Analyse
Der nordamerikanische Markt für Managementsysteme für klinische Studien ist in die USA, Kanada und Mexiko unterteilt. Das Marktwachstum ist auf die zunehmende Zahl klinischer Studien aufgrund laufender Arzneimittelentwicklungsstudien zurückzuführen. Die USA haben sich zu einem führenden Ziel für klinische Forschung entwickelt. Fast die Hälfte aller klinischen Studien wird in den USA durchgeführt. Darüber hinaus bevorzugen die meisten Pharmaforschungsunternehmen die Durchführung klinischer Studien in den USA aufgrund der etablierten medizinischen Infrastruktur, der schnellen Genehmigungsfristen, eines günstigen regulatorischen Rahmens und der weltweit akzeptierten Daten aus klinischen Studien. Einem Bericht der Weltgesundheitsorganisation (WHO) zufolge verzeichneten die USA im Jahr 2021 die höchste Anzahl klinischer Studien (157.618). Darüber hinaus wird erwartet, dass die Region Asien-Pazifik zwischen 2022 und 2030 mit der höchsten CAGR wächst.
Der Bericht stellt führende Akteure vor, die auf dem globalen Markt für Managementsysteme für klinische Studien tätig sind. Dazu gehören Advarra Inc., Clario, Deloitte Touche Tohmatsu Limited, IBM Corporation, Medideta Solution Inc., Mednet Solution Inc., Oracle Corporation, PAREXEL International Corporation, Thermo Fisher Scientific, Inc. und Veeva System Inc. Diese Akteure konzentrieren sich auf die Expansion und die Diversifizierung ihrer Marktpräsenz und die Gewinnung eines neuen Kundenstamms, um die vorherrschenden Geschäftsmöglichkeiten auf dem Markt für Managementsysteme für klinische Studien zu nutzen.
Einige Beispiele für die jüngsten Entwicklungen bei klinischen Studien Der Markt für Managementsysteme ist nachstehend aufgeführt:
- Im September 2023 ging Zelta eine Partnerschaft mit BSI Life Sciences ein, was einen wichtigen Schritt hin zur Schaffung eines nahtlosen Erlebnisses für CROs und Sponsoren darstellt Zugriff auf und Integration ihrer Daten während des gesamten klinischen Studienprozesses. Die CTMS- und eTMF-Funktionen bieten umfassende Funktionalitäten für jeden Aspekt einer klinischen Studie, vom Studienaufbau bis zum Abschluss. Zu diesen Funktionen gehören die Verwaltung und Überwachung von Standorten und Prüfärzten, vollständig integrierte Studienstammdateien (eTMF) und die Verwaltung von Studienbeständen, wodurch sie für klinische Studien weltweit zugänglich und geeignet werden.
- Im April 2022, Bristol Myers Squibb implementierte Veeva Vault CTMS weltweit und ersetzte ein herkömmliches Celgene CTMS und ein herkömmliches Bristol Myers Squibb CTMS. Veeva Vault CTMS ist jetzt eng in die eTMF- und Study Startup-Anwendungen von Veeva integriert. Durch die unternehmensweite Implementierung der branchenführenden Studienmanagement- und Überwachungslösung von Veeva möchte Bristol Myers Squibb die Studienprozesse vereinfachen und klinische Studien schneller und effizienter machen. Diese einheitliche und agile Lösung soll das End-to-End-Studienmanagement vorantreiben.
- Im Februar 2021 wurde eClinical Solutions LLC, ein globaler Anbieter von cloudbasierter Unternehmenssoftware und softwaregesteuerten klinischen Daten, gegründet Services, das Elluminate Clinical Trial Management System (CTMS) eingeführt. Die Elluminate-Plattform beschleunigt die Digitalisierung und verkürzt die Zykluszeiten für die Überprüfung klinischer Daten. Die Einführung von Elluminate CTMS ermöglichte eine schnellere und fundiertere Entscheidungsfindung.
- Historische Analyse (2 Jahre), Basisjahr, Prognose (7 Jahre) mit CAGR
- PEST- und SWOT-Analyse
- Marktgröße Wert/Volumen – Global, Regional, Land
- Branche und Wettbewerbsumfeld
- Excel-Datensatz

Report Coverage
Revenue forecast, Company Analysis, Industry landscape, Growth factors, and Trends
Segment Covered
This text is related
to segments covered.

Regional Scope
North America, Europe, Asia Pacific, Middle East & Africa, South & Central America
Country Scope
This text is related
to country scope.
Häufig gestellte Fragen
Some of the customization options available based on the request are an additional 3–5 company profiles and country-specific analysis of 3–5 countries of your choice. Customizations are to be requested/discussed before making final order confirmation#as our team would review the same and check the feasibility
The report can be delivered in PDF/PPT format; we can also share excel dataset based on the request
Integration with other technologies and adoption of AI and automation are likely to remain a key trend in the market.
Rising R&D costs and regulatory compliance are the major factors driving the clinical trial management system market.
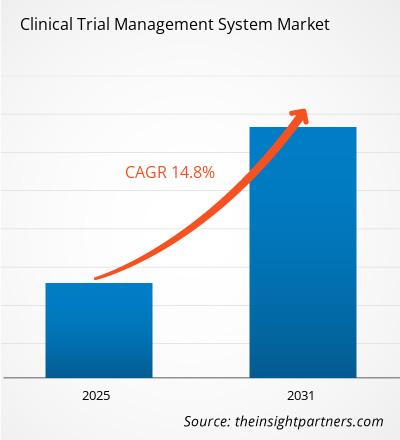
The Clinical Trial Management System Market is estimated to witness a CAGR of 14.8% from 2024 to 2031
Trends and growth analysis reports related to Technology, Media and Telecommunications : READ MORE..
The List of Companies
1. Oracle
2. Medidata Solutions Inc.
3. PAREXEL International Corporation.
4. MedNet Solutions, Inc.
5. Bioclinica
6. BioOptronics, Inc.
7. DATATRAK Int.
8. ERT Clinical
9. FORTE
10. ICON plc
The Insight Partners performs research in 4 major stages: Data Collection & Secondary Research, Primary Research, Data Analysis and Data Triangulation & Final Review.
- Data Collection and Secondary Research:
As a market research and consulting firm operating from a decade, we have published and advised several client across the globe. First step for any study will start with an assessment of currently available data and insights from existing reports. Further, historical and current market information is collected from Investor Presentations, Annual Reports, SEC Filings, etc., and other information related to company’s performance and market positioning are gathered from Paid Databases (Factiva, Hoovers, and Reuters) and various other publications available in public domain.
Several associations trade associates, technical forums, institutes, societies and organization are accessed to gain technical as well as market related insights through their publications such as research papers, blogs and press releases related to the studies are referred to get cues about the market. Further, white papers, journals, magazines, and other news articles published in last 3 years are scrutinized and analyzed to understand the current market trends.
- Primary Research:
The primarily interview analysis comprise of data obtained from industry participants interview and answers to survey questions gathered by in-house primary team.
For primary research, interviews are conducted with industry experts/CEOs/Marketing Managers/VPs/Subject Matter Experts from both demand and supply side to get a 360-degree view of the market. The primary team conducts several interviews based on the complexity of the markets to understand the various market trends and dynamics which makes research more credible and precise.
A typical research interview fulfils the following functions:
- Provides first-hand information on the market size, market trends, growth trends, competitive landscape, and outlook
- Validates and strengthens in-house secondary research findings
- Develops the analysis team’s expertise and market understanding
Primary research involves email interactions and telephone interviews for each market, category, segment, and sub-segment across geographies. The participants who typically take part in such a process include, but are not limited to:
- Industry participants: VPs, business development managers, market intelligence managers and national sales managers
- Outside experts: Valuation experts, research analysts and key opinion leaders specializing in the electronics and semiconductor industry.
Below is the breakup of our primary respondents by company, designation, and region:
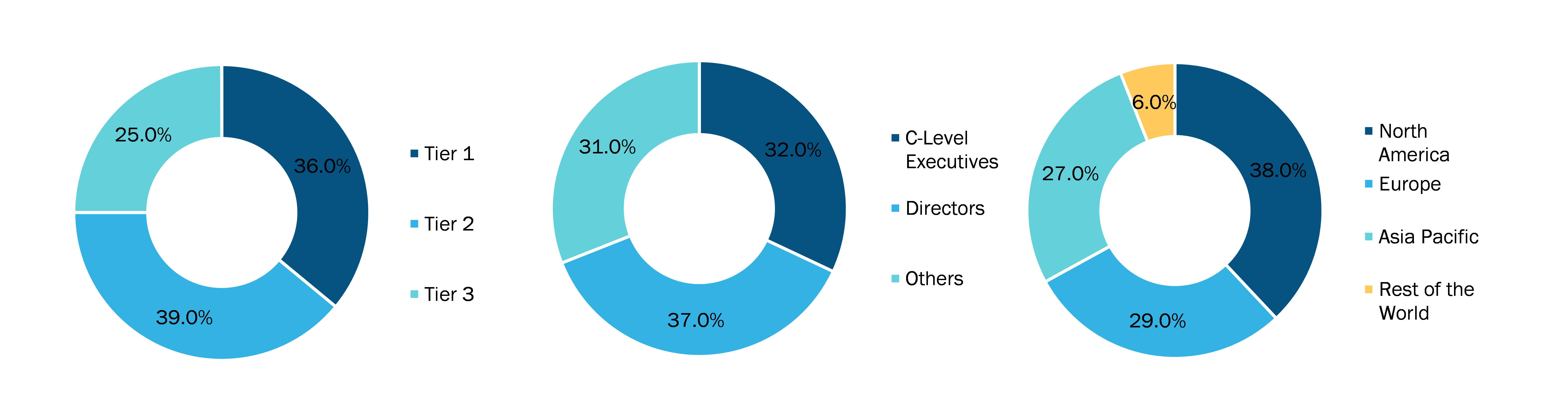
Once we receive the confirmation from primary research sources or primary respondents, we finalize the base year market estimation and forecast the data as per the macroeconomic and microeconomic factors assessed during data collection.
- Data Analysis:
Once data is validated through both secondary as well as primary respondents, we finalize the market estimations by hypothesis formulation and factor analysis at regional and country level.
- Macro-Economic Factor Analysis:
We analyse macroeconomic indicators such the gross domestic product (GDP), increase in the demand for goods and services across industries, technological advancement, regional economic growth, governmental policies, the influence of COVID-19, PEST analysis, and other aspects. This analysis aids in setting benchmarks for various nations/regions and approximating market splits. Additionally, the general trend of the aforementioned components aid in determining the market's development possibilities.
- Country Level Data:
Various factors that are especially aligned to the country are taken into account to determine the market size for a certain area and country, including the presence of vendors, such as headquarters and offices, the country's GDP, demand patterns, and industry growth. To comprehend the market dynamics for the nation, a number of growth variables, inhibitors, application areas, and current market trends are researched. The aforementioned elements aid in determining the country's overall market's growth potential.
- Company Profile:
The “Table of Contents” is formulated by listing and analyzing more than 25 - 30 companies operating in the market ecosystem across geographies. However, we profile only 10 companies as a standard practice in our syndicate reports. These 10 companies comprise leading, emerging, and regional players. Nonetheless, our analysis is not restricted to the 10 listed companies, we also analyze other companies present in the market to develop a holistic view and understand the prevailing trends. The “Company Profiles” section in the report covers key facts, business description, products & services, financial information, SWOT analysis, and key developments. The financial information presented is extracted from the annual reports and official documents of the publicly listed companies. Upon collecting the information for the sections of respective companies, we verify them via various primary sources and then compile the data in respective company profiles. The company level information helps us in deriving the base number as well as in forecasting the market size.
- Developing Base Number:
Aggregation of sales statistics (2020-2022) and macro-economic factor, and other secondary and primary research insights are utilized to arrive at base number and related market shares for 2022. The data gaps are identified in this step and relevant market data is analyzed, collected from paid primary interviews or databases. On finalizing the base year market size, forecasts are developed on the basis of macro-economic, industry and market growth factors and company level analysis.
- Data Triangulation and Final Review:
The market findings and base year market size calculations are validated from supply as well as demand side. Demand side validations are based on macro-economic factor analysis and benchmarks for respective regions and countries. In case of supply side validations, revenues of major companies are estimated (in case not available) based on industry benchmark, approximate number of employees, product portfolio, and primary interviews revenues are gathered. Further revenue from target product/service segment is assessed to avoid overshooting of market statistics. In case of heavy deviations between supply and demand side values, all thes steps are repeated to achieve synchronization.
We follow an iterative model, wherein we share our research findings with Subject Matter Experts (SME’s) and Key Opinion Leaders (KOLs) until consensus view of the market is not formulated – this model negates any drastic deviation in the opinions of experts. Only validated and universally acceptable research findings are quoted in our reports.
We have important check points that we use to validate our research findings – which we call – data triangulation, where we validate the information, we generate from secondary sources with primary interviews and then we re-validate with our internal data bases and Subject matter experts. This comprehensive model enables us to deliver high quality, reliable data in shortest possible time.
 Holen Sie sich ein kostenloses Muster für diesen Bericht
Holen Sie sich ein kostenloses Muster für diesen Bericht