Der europäische Markt für Pharmakovigilanz- und Arzneimittelsicherheitssoftware wurde im Jahr 2023 auf 52,37 Millionen US-Dollar geschätzt und soll bis 2031 84,66 Millionen US-Dollar erreichen; für den Zeitraum 2023–2031 wird eine durchschnittliche jährliche Wachstumsrate von 6,2 % erwartet. Cloudbasierte Pharmakovigilanz- und Arzneimittelsicherheitssoftware dürfte in den kommenden Jahren neue wichtige Trends auf den Markt bringen.
Marktanalyse für Pharmakovigilanz- und Arzneimittelsicherheitssoftware in Europa
Software für Pharmakovigilanz und Arzneimittelsicherheit sorgt für eine schnelle Erkennung und Bewertung von Nebenwirkungen im Zusammenhang mit Medikamenten. Durch eine verbesserte Sicherheitsüberwachung und die Automatisierung der Datenerfassung und -analyse beschleunigt die Software die Identifizierung potenzieller Sicherheitsbedenken und ermöglicht ein schnelles Eingreifen zur Risikominderung. Dieser proaktive Ansatz verbessert die Einhaltung gesetzlicher Vorschriften, die Patientensicherheit und die allgemeinen Ergebnisse im Bereich der öffentlichen Gesundheit. Darüber hinaus bietet Software für Pharmakovigilanz und Arzneimittelsicherheit mit erweiterten Analyse- und Echtzeitüberwachungsfunktionen einen starken Rahmen für die Optimierung der Arzneimittelsicherheitsüberwachung. Die Integration von KI und prädiktiver Analyse mit Software für Pharmakovigilanz und Arzneimittelsicherheit verbessert die Fähigkeit, potenzielle Sicherheitsrisiken zu identifizieren, bevor sie zu ernsthaften Problemen eskalieren. Diese fortschrittlichen Technologien helfen bei der Analyse großer Mengen strukturierter und unstrukturierter Daten, um kommende Sicherheitssignale und -trends zu erkennen, was proaktive Strategien zur Risikominderung auslöst. Aufgrund verschiedener Vorteile steigt daher die Nachfrage nach Software für Pharmakovigilanz und Arzneimittelsicherheit in Europa.
Überblick über den europäischen Markt für Pharmakovigilanz- und Arzneimittelsicherheitssoftware
Pharmakovigilanz ist die Wissenschaft der Wahrung der öffentlichen Gesundheit durch Gewährleistung der Sicherheit und Wirksamkeit pharmazeutischer Produkte. Software für Pharmakovigilanz und Arzneimittelsicherheit ist ein wichtiges Instrument, das Fehler bei der manuellen Dateneingabe, die überwältigende Menge an Sicherheitsdaten und verschiedene andere Herausforderungen behebt. Von klinischen Studien bis zur Überwachung nach der Markteinführung ist diese Software während des gesamten Lebenszyklus der Arzneimittelentwicklung unverzichtbar. Software für Pharmakovigilanz und Arzneimittelsicherheit trägt dazu bei, die Bearbeitungszeit für unerwünschte Ereignisse zu verkürzen und die Patientensicherheit durch frühzeitige Signalerkennung zu verbessern. Angesichts der Weiterentwicklung der Vorschriften und der Intensivierung der europäischen Zusammenarbeit ist die Einführung von Software für Pharmakovigilanz und Arzneimittelsicherheit vorteilhaft und daher für Pharmaunternehmen und Aufsichtsbehörden unverzichtbar. Im Jahr 2022 hat das Pharmaceutical Inspection Co-operation Scheme (PIC/S) seine Richtlinien zur Pharmakovigilanz aktualisiert, um internationalen Standards zu entsprechen, und dabei die Bedeutung einer robusten Software für Pharmakovigilanz und Arzneimittelsicherheit hervorgehoben. Darüber hinaus gewährleistet die Software die Einhaltung regulatorischer Standards, indem sie die Erstellung umfassender Sicherheitsberichte und die Einreichung bei den Aufsichtsbehörden erleichtert, was den Unternehmen hilft, Strafen zu vermeiden und ihren Ruf zu wahren.
Passen Sie die Forschung Ihren Anforderungen an
Wir können die Analyse und den Umfang optimieren und anpassen, die unsere Standardangebote nicht abdecken. Diese Flexibilität hilft Ihnen, genau die Informationen zu erhalten, die Sie für Ihre Geschäftsplanung und Entscheidungsfindung benötigen.
Europäischer Markt für Pharmakovigilanz- und Arzneimittelsicherheitssoftware:
CAGR (2023 - 2031)6,2 %- Marktgröße 2023
52,37 Millionen US-Dollar - Marktgröße 2031
84,66 Millionen US-Dollar

Marktdynamik
- Anstieg der Fälle unerwünschter Arzneimittelwirkungen
- Globalisierung der Pharmakovigilanz
- Anstieg der Arzneimittelentwicklungsraten
- Cloudbasierte Pharmakovigilanz
- Software zur Arzneimittelsicherheit
- Integration von Software mit KI, ML
- NLP
Schlüsselspieler
- ArisEurope
- ICON plc Syneos Health
- Accenture
- IQVIA
- Genpact
- Bewusst
- Paraxel International Corporation
- Beteiligungen an der Laboratory Corporation of America
- Maximale Anwendung
- Clinevo-Technologien
Regionaler Überblick
- Europa
Marktsegmentierung
 Angebot
Angebot- Software
- Dienstleistungen
 Einsatz
Einsatz- Wolke
- Vor Ort
 Unternehmensgröße
Unternehmensgröße- Große Unternehmen
- KMU
 Bilden
Bilden- Standard
- Individuell
- Das Beispiel-PDF zeigt die Inhaltsstruktur und die Art der Informationen mit qualitativer und quantitativer Analyse.
Treiber und Chancen auf dem europäischen Markt für Pharmakovigilanz- und Arzneimittelsicherheitssoftware
Anstieg der Fälle unerwünschter Arzneimittelwirkungen
In Europa können unerwünschte Arzneimittelwirkungen (UAW) eine bedeutende Todes- und Krankheitsursache sein. Da alle Arzneimittel unerwünschte Arzneimittelwirkungen haben können, ist bei jeder Verschreibung eines Arzneimittels eine Risiko-Nutzen-Analyse erforderlich. UAW bleiben im modernen Gesundheitswesen eine Herausforderung, insbesondere angesichts der zunehmenden Komplexität der Therapeutika, der alternden Bevölkerung und der zunehmenden Multimorbidität in Europa. Mithilfe von Pharmakovigilanzsoftware können Gesundheitsdienstleister und Pharmaunternehmen Daten zu UAW systematisch erfassen, analysieren und melden und die damit verbundenen Herausforderungen bewältigen.
ADRs sind eine der Hauptursachen für die steigenden Sterberaten in Europa. Laut dem Bericht der Europäischen Drogenagentur (EUDA) betrug die Sterberate in der Europäischen Union im Jahr 2021 in Bezug auf Überdosierungen ~18,3 Todesfälle pro Million Einwohner im Alter von 15 bis 64 Jahren. Außerdem gab es in der Europäischen Union im Jahr 2021 mindestens 6.166 Todesfälle durch Überdosierungen illegaler Drogen (5.796 im Jahr 2020). Diese Gesamtzahl erreichte ~6.677 Todesfälle, wenn Norwegen und die Türkei einbezogen wurden (6.434 im Jahr 2020).
Da immer mehr Nebenwirkungen gemeldet und erkannt werden, stehen Pharmaunternehmen , Gesundheitsdienstleister und Aufsichtsbehörden unter größerem Druck, die Überwachungs- und Meldeprozesse für die Arzneimittelsicherheit zu verbessern. Dies erfordert die Einführung von Software für die Pharmakovigilanz und Arzneimittelsicherheit, um das wachsende Volumen an Sicherheitsdaten zu sammeln, zu analysieren und zu verwalten. Diese Software hilft dabei, den Prozess der Erkennung, Bewertung und Vorbeugung von Nebenwirkungen zu optimieren und ermöglicht schnellere Reaktionszeiten und genauere Risikobewertungen. Somit treibt die steigende Zahl unerwünschter Arzneimittelwirkungen das Wachstum des europäischen Marktes für Software für die Pharmakovigilanz und Arzneimittelsicherheit an .
Integration von Software mit KI, ML und NLP
Künstliche Intelligenz (KI), maschinelles Lernen (ML), Verarbeitung natürlicher Sprache (NLP) und andere Technologien verändern die ressourcenintensiven Arbeitslasten der Pharmakovigilanz und sorgen für einen fundierteren und effizienteren Ansatz. Softwareplattformen für Pharmakovigilanz und Arzneimittelsicherheit sind meist mit erweiterten Analyse- und KI-Funktionen ausgestattet, die die Erkennung von Sicherheitssignalen verbessern. Diese Tools können riesige Datenmengen analysieren und Korrelationen und Muster identifizieren, die bei herkömmlichen Methoden möglicherweise übersehen werden. KI-gesteuerte prädiktive Analysen können auch potenzielle Sicherheitsprobleme vorhersagen, sodass Unternehmen proaktive Maßnahmen ergreifen können. ML-Modelle werden genutzt, um potenzielle Nebenwirkungen im Zusammenhang mit der Einnahme von Medikamenten vorherzusagen. Beispielsweise nutzen Pharmakovigilanzkampagnen ML, um riesige Datensätze zu durchforsten und Muster zu erkennen, die auf ein Risiko für unerwünschte Arzneimittelwirkungen hinweisen könnten. ML-Algorithmen sind besonders gut im Umgang mit unstrukturierten Daten wie sozialen Medien und Patientenakten, um Sicherheitsbedenken vorherzusagen.
KI-Systeme werden zunehmend eingesetzt, um die Echtzeitüberwachung der Arzneimittelsicherheit voranzutreiben. Diese proaktive Überwachung umfasst Daten aus klinischen Studien, das Durchsuchen medizinischer Literatur und Patientenregister nach unerwünschten Ereignissen (AEs); sie kann auch die Genauigkeit und Geschwindigkeit der ADR-Erkennung verbessern. Darüber hinaus können KI-Systeme mithilfe von NLP relevante Informationen wie Medikamentennamen und Symptome aus riesigen Textdatensätzen extrahieren und so eine genaue und schnelle Meldung unerwünschter Ereignisse ermöglichen. Dies beschleunigt die Identifizierung unbekannter oder neuer Arzneimittelsicherheitsprobleme und trägt so erheblich zu Fortschritten bei der Pharmakovigilanz bei. Verschiedene Unternehmen bieten KI-basierte Software für Pharmakovigilanz und Arzneimittelsicherheit an, darunter ArisGlobal. Daher wird erwartet, dass die Integration von Software für Pharmakovigilanz und Arzneimittelsicherheit mit KI, ML und NLP im Prognosezeitraum lukrative Möglichkeiten für das Marktwachstum schaffen wird.pharmacovigilance efforts. Various companies offer AI-based pharmacovigilance and drug safety software, including ArisGlobal. Thus, the integration of pharmacovigilance and drug safety software with AI, ML, and NLP is expected to create lucrative opportunities for the market growth during the forecast period.
Segmentierungsanalyse des europäischen Marktberichts zu Pharmakovigilanz- und ArzneimittelsicherheitssoftwarePharmacovigilance and Drug Safety Software Market Report Segmentation Analysis
Wichtige Segmente, die zur Ableitung der europäischen Marktanalyse für Pharmakovigilanz- und Arzneimittelsicherheitssoftware beigetragen haben, sind Angebot, Organisationsgröße, Bereitstellung, Form, Funktionalität und Endbenutzer.pharmacovigilance and drug safety software market analysis are offerings, organization size, deployment, form, functionality, and end user.
- Basierend auf der Unternehmensgröße ist der europäische Markt für Pharmakovigilanz- und Arzneimittelsicherheitssoftware in Großunternehmen und KMU unterteilt. Das Segment der Großunternehmen dominierte den Markt im Jahr 2023.
- Angebotsmäßig ist der Markt in Software und Dienstleistungen unterteilt. Das Softwaresegment hatte im Jahr 2023 einen größeren Marktanteil.
- Basierend auf der Bereitstellung ist der europäische Markt für Pharmakovigilanz- und Arzneimittelsicherheitssoftware in Cloud und On-Premises unterteilt. Das Cloud-Segment dominierte den Markt im Jahr 2023
- Basierend auf der Form ist der europäische Markt für Pharmakovigilanz- und Arzneimittelsicherheitssoftware in Standard- und kundenspezifische Software unterteilt. Das Standardsegment dominierte den Markt im Jahr 2023.
- Nach Funktionalität ist der europäische Markt für Pharmakovigilanz- und Arzneimittelsicherheitssoftware in Fallmanagement, Signal- und Risikomanagement, Qualität und Compliance, Auditunterstützung und Schulungscompliance, Problemverfolgung und Verfolgung unerwünschter Ereignisse, klinisches Sicherheitsmanagement und Sicherheit klinischer Studien, medizinisches Schreiben, Gesundheitsanalytik und andere unterteilt. Das Segment Signal- und Risikomanagement hatte im Jahr 2023 den größten Marktanteil.
- Basierend auf dem Endnutzer ist der europäische Markt für Pharmakovigilanz- und Arzneimittelsicherheitssoftware in Pharma- und Biotechnologieunternehmen, Auftragsforschungsinstitute, Unternehmen zur Auslagerung von Geschäftsprozessen und andere Pharmakovigilanzdienstleister segmentiert. Das Segment der Pharma- und Biotechnologieunternehmen dominierte den Markt im Jahr 2023.
Marktanteilsanalyse für Pharmakovigilanz- und Arzneimittelsicherheitssoftware in Europa nach geografischen Gesichtspunkten
Der europäische Markt für Pharmakovigilanz- und Arzneimittelsicherheitssoftware ist in Frankreich, Deutschland, Italien, Spanien, Großbritannien und den Rest Europas unterteilt. Die steigende Nachfrage nach Pharmakovigilanz- und Arzneimittelsicherheitssoftware in Europa wird auf verschiedene Faktoren zurückgeführt, darunter behördliche Vorschriften, zunehmende Arzneimittelzulassungen, wachsende Bedeutung der Patientensicherheit und technologische Fortschritte. Das Pharmakovigilanzsystem der EU ist eines der fortschrittlichsten der Welt. Die Europäische Arzneimittel-Agentur (EMA) und andere Aufsichtsbehörden legen strenge Anforderungen an die Pharmakovigilanz fest, die die Einführung fortschrittlicher Softwarelösungen erforderlich machen. So haben beispielsweise die Einführung der EU-Pharmakovigilanzrichtlinie (2010/84/EU) und der nachfolgenden Verordnung (EU) Nr. 1235/2010 strengere Regeln für die Überwachung unerwünschter Arzneimittelwirkungen (UAW) eingeführt. Unternehmen müssen Sicherheitsdaten in Echtzeit melden, was die Nachfrage nach effizienten Softwaresystemen, die große Datenmengen verarbeiten können, deutlich erhöht.
Umfang des Marktberichts zu Pharmakovigilanz- und Arzneimittelsicherheitssoftware für Europa
| Berichtsattribut | Details |
|---|---|
| Marktgröße im Jahr 2023 | 52,37 Millionen US-Dollar |
| Marktgröße bis 2031 | 84,66 Millionen US-Dollar |
| Globale CAGR (2023 - 2031) | 6,2 % |
| Historische Daten | 2021-2022 |
| Prognosezeitraum | 2024–2031 |
| Abgedeckte Segmente | Durch das Angebot
|
| Abgedeckte Regionen und Länder | Europa
|
| Marktführer und wichtige Unternehmensprofile |
|
- Das Beispiel-PDF zeigt die Inhaltsstruktur und die Art der Informationen mit qualitativer und quantitativer Analyse.
Neuigkeiten und aktuelle Entwicklungen zum europäischen Markt für Pharmakovigilanz- und Arzneimittelsicherheitssoftware
Der europäische Markt für Pharmakovigilanz- und Arzneimittelsicherheitssoftware wird durch die Erhebung qualitativer und quantitativer Daten nach Primär- und Sekundärforschung bewertet, die wichtige Unternehmensveröffentlichungen, Verbandsdaten und Datenbanken umfasst. Nachfolgend sind einige der wichtigsten Entwicklungen auf dem europäischen Markt für Pharmakovigilanz- und Arzneimittelsicherheitssoftware aufgeführt:
- ArisGlobal – ein Marktführer für globale Technologielösungen zur Arzneimittelentwicklung – gab bekannt, dass sich Medac, ein in Deutschland ansässiger Pharmahersteller, der auf die Bereiche Onkologie und Hämatologie, Urologie und Autoimmunerkrankungen spezialisiert ist, für LifeSphere Safety entschieden hat, um seine Arzneimittelsicherheitsprozesse zu modernisieren. Präzise, patienten- und bevölkerungsspezifische Analysen sind entscheidend, um die Behandlungsrisiken für Patienten zu minimieren und so das bestmögliche Behandlungsergebnis zu erzielen. (Quelle: ArisGlobal, Pressemitteilung, Mai 2023)
- IQVIA, ein weltweit führender Anbieter von fortschrittlichen Analyse- und Technologielösungen sowie klinischen Forschungsdienstleistungen für die Biowissenschaftsbranche, gab eine strategische Zusammenarbeit mit Argenx bekannt, um die Behandlung von Patienten mit seltenen Autoimmunerkrankungen durch innovative und integrierte technologiegestützte Pharmakovigilanz-Sicherheitsdienste und -lösungen zu verbessern. (Quelle: IQVIA, Pressemitteilung, Januar 2023)
Umfang und Ergebnisse des europäischen Marktberichts zu Software für Pharmakovigilanz und Arzneimittelsicherheit
Die „Marktgröße und Prognose für Pharmakovigilanz- und Arzneimittelsicherheitssoftware in Europa (2021–2031)“ bietet eine detaillierte Analyse des Marktes, die die unten genannten Bereiche abdeckt:
- Größe und Prognose des europäischen Marktes für Pharmakovigilanz- und Arzneimittelsicherheitssoftware auf Länderebene für alle wichtigen Marktsegmente, die im Rahmen des Programms abgedeckt sind
- Markttrends für Pharmakovigilanz- und Arzneimittelsicherheitssoftware in Europa sowie Marktdynamiken wie Treiber, Beschränkungen und wichtige Chancen
- Detaillierte PEST- und SWOT-Analyse
- Analyse des europäischen Marktes für Pharmakovigilanz- und Arzneimittelsicherheitssoftware mit Blick auf wichtige Markttrends, regionale Rahmenbedingungen, wichtige Akteure, Vorschriften und aktuelle Marktentwicklungen
- Branchenlandschaft und Wettbewerbsanalyse, einschließlich Marktkonzentration, Heatmap-Analyse, prominenten Akteuren und aktuellen Entwicklungen für den europäischen Markt für Pharmakovigilanz- und Arzneimittelsicherheitssoftware
- Detaillierte Firmenprofile
- Historische Analyse (2 Jahre), Basisjahr, Prognose (7 Jahre) mit CAGR
- PEST- und SWOT-Analyse
- Marktgröße Wert/Volumen – Global, Regional, Land
- Branche und Wettbewerbsumfeld
- Excel-Datensatz

Report Coverage
Revenue forecast, Company Analysis, Industry landscape, Growth factors, and Trends
Segment Covered
This text is related
to segments covered.

Regional Scope
North America, Europe, Asia Pacific, Middle East & Africa, South & Central America
Country Scope
This text is related
to country scope.
Häufig gestellte Fragen
The Europe pharmacovigilance and drug safety software market was estimated to be US$ 52.37 million in 2023 and is expected to grow at a CAGR of 6.2% during the forecast period 2023 - 2031.
Cloud-based pharmacovigilance and drug safety software, which is anticipated to play a significant role in the Europe pharmacovigilance and drug safety software market in the coming years.
Rise in incidences of adverse drug reactions, globalization of pharmacovigilance, surge in drug development rates are the major factors that propel the Europe pharmacovigilance and drug safety software market.
The key players holding majority shares in the Europe pharmacovigilance and drug safety software market are ArisEurope, ICON plc, Syneos Health, Accenture, IQVIA, Genpact, Cognizant, Paraxel International Corporation, Laboratory Corporation of America Holdings, Max Application, Clinevo Technologies, Qinecsa Solutions, AB Cube, and Veeva Systems.
The incremental growth expected to be recorded for the Europe pharmacovigilance and drug safety software market during the forecast period is US$ 32.29 million.
The Europe pharmacovigilance and drug safety software market is expected to reach US$ 84.66 million by 2031.
Trends and growth analysis reports related to Technology, Media and Telecommunications : READ MORE..
The List of Companies - Europe Pharmacovigilance and Drug Safety Software Market
- ArisGlobal LLC
- Max Application
- Oracle Corp
- Veeva Systems Inc
- IQVIA Holdings Inc
- ICON Plc
- Cognizant Technology Solutions Corp
- Accenture Plc
- Syneos Health Inc
- Genpact Ltd.
- AB Cube S.A.S.
- Laboratory Corp of America Holdings
- Parexel International Corp
- Qinecsa Solutions
- Clinevo Technologies
The Insight Partners performs research in 4 major stages: Data Collection & Secondary Research, Primary Research, Data Analysis and Data Triangulation & Final Review.
- Data Collection and Secondary Research:
As a market research and consulting firm operating from a decade, we have published and advised several client across the globe. First step for any study will start with an assessment of currently available data and insights from existing reports. Further, historical and current market information is collected from Investor Presentations, Annual Reports, SEC Filings, etc., and other information related to company’s performance and market positioning are gathered from Paid Databases (Factiva, Hoovers, and Reuters) and various other publications available in public domain.
Several associations trade associates, technical forums, institutes, societies and organization are accessed to gain technical as well as market related insights through their publications such as research papers, blogs and press releases related to the studies are referred to get cues about the market. Further, white papers, journals, magazines, and other news articles published in last 3 years are scrutinized and analyzed to understand the current market trends.
- Primary Research:
The primarily interview analysis comprise of data obtained from industry participants interview and answers to survey questions gathered by in-house primary team.
For primary research, interviews are conducted with industry experts/CEOs/Marketing Managers/VPs/Subject Matter Experts from both demand and supply side to get a 360-degree view of the market. The primary team conducts several interviews based on the complexity of the markets to understand the various market trends and dynamics which makes research more credible and precise.
A typical research interview fulfils the following functions:
- Provides first-hand information on the market size, market trends, growth trends, competitive landscape, and outlook
- Validates and strengthens in-house secondary research findings
- Develops the analysis team’s expertise and market understanding
Primary research involves email interactions and telephone interviews for each market, category, segment, and sub-segment across geographies. The participants who typically take part in such a process include, but are not limited to:
- Industry participants: VPs, business development managers, market intelligence managers and national sales managers
- Outside experts: Valuation experts, research analysts and key opinion leaders specializing in the electronics and semiconductor industry.
Below is the breakup of our primary respondents by company, designation, and region:
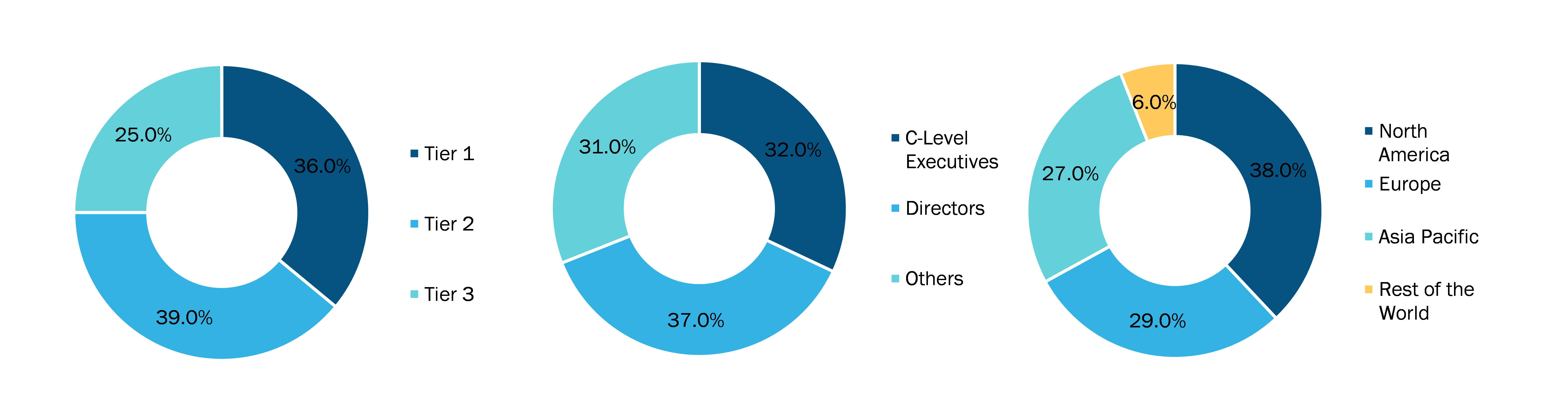
Once we receive the confirmation from primary research sources or primary respondents, we finalize the base year market estimation and forecast the data as per the macroeconomic and microeconomic factors assessed during data collection.
- Data Analysis:
Once data is validated through both secondary as well as primary respondents, we finalize the market estimations by hypothesis formulation and factor analysis at regional and country level.
- Macro-Economic Factor Analysis:
We analyse macroeconomic indicators such the gross domestic product (GDP), increase in the demand for goods and services across industries, technological advancement, regional economic growth, governmental policies, the influence of COVID-19, PEST analysis, and other aspects. This analysis aids in setting benchmarks for various nations/regions and approximating market splits. Additionally, the general trend of the aforementioned components aid in determining the market's development possibilities.
- Country Level Data:
Various factors that are especially aligned to the country are taken into account to determine the market size for a certain area and country, including the presence of vendors, such as headquarters and offices, the country's GDP, demand patterns, and industry growth. To comprehend the market dynamics for the nation, a number of growth variables, inhibitors, application areas, and current market trends are researched. The aforementioned elements aid in determining the country's overall market's growth potential.
- Company Profile:
The “Table of Contents” is formulated by listing and analyzing more than 25 - 30 companies operating in the market ecosystem across geographies. However, we profile only 10 companies as a standard practice in our syndicate reports. These 10 companies comprise leading, emerging, and regional players. Nonetheless, our analysis is not restricted to the 10 listed companies, we also analyze other companies present in the market to develop a holistic view and understand the prevailing trends. The “Company Profiles” section in the report covers key facts, business description, products & services, financial information, SWOT analysis, and key developments. The financial information presented is extracted from the annual reports and official documents of the publicly listed companies. Upon collecting the information for the sections of respective companies, we verify them via various primary sources and then compile the data in respective company profiles. The company level information helps us in deriving the base number as well as in forecasting the market size.
- Developing Base Number:
Aggregation of sales statistics (2020-2022) and macro-economic factor, and other secondary and primary research insights are utilized to arrive at base number and related market shares for 2022. The data gaps are identified in this step and relevant market data is analyzed, collected from paid primary interviews or databases. On finalizing the base year market size, forecasts are developed on the basis of macro-economic, industry and market growth factors and company level analysis.
- Data Triangulation and Final Review:
The market findings and base year market size calculations are validated from supply as well as demand side. Demand side validations are based on macro-economic factor analysis and benchmarks for respective regions and countries. In case of supply side validations, revenues of major companies are estimated (in case not available) based on industry benchmark, approximate number of employees, product portfolio, and primary interviews revenues are gathered. Further revenue from target product/service segment is assessed to avoid overshooting of market statistics. In case of heavy deviations between supply and demand side values, all thes steps are repeated to achieve synchronization.
We follow an iterative model, wherein we share our research findings with Subject Matter Experts (SME’s) and Key Opinion Leaders (KOLs) until consensus view of the market is not formulated – this model negates any drastic deviation in the opinions of experts. Only validated and universally acceptable research findings are quoted in our reports.
We have important check points that we use to validate our research findings – which we call – data triangulation, where we validate the information, we generate from secondary sources with primary interviews and then we re-validate with our internal data bases and Subject matter experts. This comprehensive model enables us to deliver high quality, reliable data in shortest possible time.
 Holen Sie sich ein kostenloses Muster für diesen Bericht
Holen Sie sich ein kostenloses Muster für diesen Bericht