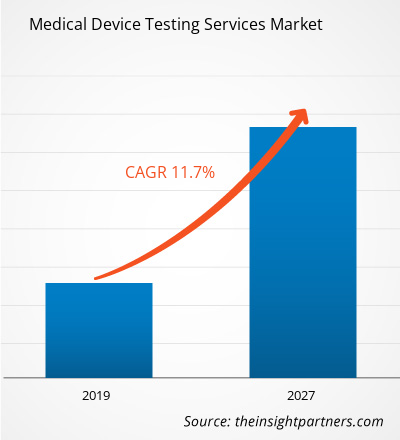
Der Markt für Prüfdienstleistungen für medizinische Geräte im Gesundheitswesen hatte im Jahr 2018 einen Wert von 5.505,4 Millionen US-Dollar und soll bis 2027 einen Wert von 14.660,1 Millionen US-Dollar erreichen; von 2019 bis 2027 dürfte er mit einer durchschnittlichen jährlichen Wachstumsrate von 11,7 % wachsen.CAGR of 11.7% from 2019 to 2027.
Medizinische Geräte sind sehr wichtig, da sie einen direkten Einfluss auf das Leben der Patienten haben. Um den Patienten ein qualitativ hochwertiges und sicheres Erlebnis zu bieten, testen Hersteller medizinischer Geräte diese, bevor sie sie auf den Markt bringen. Hersteller medizinischer Geräte führen die Tests lieber selbst durch oder lagern die Testdienstleistungen an Auftragsforschungsinstitute (CROs) aus, um die strengen gesetzlichen Richtlinien einzuhalten. Die Prüfung der medizinischen Geräte soll die Sicherheit, Qualität und Konsistenz der Dienste während aller Phasen der Entwicklung und Verwendung medizinischer Geräte gewährleisten. Die medizinische Behandlung ist in hohem Maße von medizinischen Geräten abhängig, daher ist es wichtig, sicherzustellen, dass die Tests medizinischer Geräte mit höchster Kompetenz durchgeführt werden. Das Wachstum der Testdienstleistungen für medizinische Geräte im Gesundheitsmarkt ist auf die innovative Produktentwicklung zurückzuführen. Kooperationen, Fusionen und Übernahmen sowie strenge regulatorische Rahmenbedingungen für die Zulassung medizinischer Geräte kurbeln das Wachstum des Marktes im Laufe der Jahre an. Auch die Entwicklungen in der Medizingerätebranche werden sich im Prognosezeitraum wahrscheinlich positiv auf die Nachfrage nach dem Markt auswirken. Das Wachstum des Marktes wird jedoch durch Faktoren wie Unterbrechungen vertraglicher Verpflichtungen gebremst.
Der Markt für Prüfdienste für medizinische Geräte im Gesundheitswesen dürfte nach der Pandemie ein erhebliches Wachstum verzeichnen. SGS SA, Eurofins, Toxikon, Pace Analytical Services, LLC, Intertek Group plc, NORTH AMERICAN SCIENCE ASSOCIATES INC., Charles River, WuXi AppTec, Element Materials Technology, TÜV SÜD AG mRNA wird voraussichtlich auftauchen und die Pharmaindustrie verändern, und es wird erwartet, dass der Markt in den kommenden Jahren auch mehr vertikale Integration und Joint Ventures erleben wird.
Markteinblicke
Zunehmende Anwendung von Prüfdiensten für medizinische Geräte im Gesundheitswesen fördert das Wachstum des Marktes für Prüfdienste für medizinische Geräte im Gesundheitswesen
Passen Sie diesen Bericht Ihren Anforderungen an
Sie erhalten kostenlos individuelle Anpassungen an jedem Bericht, einschließlich Teilen dieses Berichts oder einer Analyse auf Länderebene, eines Excel-Datenpakets sowie tolle Angebote und Rabatte für Start-ups und Universitäten.
- Holen Sie sich die wichtigsten Markttrends aus diesem Bericht.Dieses KOSTENLOSE Beispiel umfasst eine Datenanalyse von Markttrends bis hin zu Schätzungen und Prognosen.
Das Testen von Medizinprodukten erfordert umfassende Erfahrung in der Branche, in den nationalen und nationalen Gesetzen sowie Informationen über die Geräte, die Infrastruktur und die Fähigkeit, das Testen zu unterstützen. Die Gesundheits- und Medizinproduktebranche ist aufgrund kontinuierlicher Entwicklung und fortschrittlicher Lösungen sehr aktiv. Die Verbesserungen in der Medizinproduktetechnologie haben die Effizienz der Patientenversorgung in den letzten Jahrzehnten deutlich verbessert.
Allerdings stehen Hersteller verschiedener Medizinprodukte manchmal vor Herausforderungen, wenn es darum geht, ihre Produkte marktreif zu machen. Die Vorschriften sind manchmal komplex und schwer zu verstehen, vor allem wenn es um die Anwendung innovativer und neuartiger Medizinprodukte geht.
Ein Rückruf ist ein Prozess zur Entfernung oder Änderung von Produkten, die nicht den von der Food and Drug Administration (FDA) erlassenen Gesetzen entsprechen. Die Rückrufe von Medizinprodukten werden meist freiwillig von den Unternehmen gemäß 21 CFR 7 durchgeführt. Die Produktrückrufe werden von der FDA in verschiedene Kategorien eingeteilt, beispielsweise I, II oder III, um den relativen Grad der Gesundheitsgefährdung anzugeben, den das zurückgerufene Produkt darstellt.
Laut FDA wurden 2018 seit 2008 über 80.000 Vorfälle aufgrund von Verletzungen durch medizinische Geräte festgestellt. Seit einigen Jahren haben Medizingerätehersteller und Ärzte festgestellt, dass Rückenmarkstimulatoren Patienten mit Schmerzstörungen helfen. Aus diesem Grund sind sie zu einem der am stärksten wachsenden Produkte in der 400 Milliarden Dollar schweren Medizingerätebranche geworden. Die zunehmende Anzahl von Produktrückrufen und die höhere Nachfrage nach Qualitätsprodukten erhöhen daher den Bedarf an Tests für Medizingeräte. Dies wird den Markt für Testdienstleistungen für Medizingeräte ankurbeln.
Die Medizintechnik verbessert das Leben, indem sie Krankheiten frühzeitig erkennt und Behandlung, Diagnose und Patientenüberwachung verbessert. Schulungsprogramme für kleine und mittlere Unternehmen (KMU) wurden in Ländern wie China, Chile, Indonesien, Mexiko, Malaysia, Singapur, den Philippinen, Peru, Russland und Vietnam und anderen umgesetzt. Im Jahr 2018 wurde der Markt für Medizingeräte in Großbritannien auf etwa 10,6 Milliarden US-Dollar geschätzt. Darunter sind etwa 2.500 kleine bis mittelgroße Medizingeräteunternehmen in Großbritannien. Darüber hinaus haben zahlreiche multinationale Unternehmen ihren Hauptsitz oder ihre Tochtergesellschaften im Land. Darüber hinaus geben die Akutkliniken jedes Jahr durchschnittlich etwa 6,6 Milliarden US-Dollar für klinische Bedarfsartikel aus, zu denen auch medizinische Geräte gehören.
Darüber hinaus gab die International Trade Administration (ITA) im Jahr 2018 an, dass es in Frankreich über 1.300 Medizintechnikunternehmen gibt, von denen ein Drittel aller Medizintechnikunternehmen ausländische Unternehmen sind. Diese ausländischen Medizintechnikunternehmen machen jedoch etwa zwei Drittel des Gesamtgeschäfts aus.
Darüber hinaus sind etwa 92 % der 1.300 Medizinproduktehersteller in Frankreich kleine und mittlere Unternehmen (KMU), von denen 88 % ausschließlich Medizinprodukte herstellen. KMU lagern die Tests von Medizinprodukten aus, da dies hohe Kosten, Zeit und Facharbeit erfordert.
Darüber hinaus entfallen auf Madrid und Katalonien mehr als 80 Prozent des Medizinprodukteumsatzes. Davon entfallen 90 Prozent des Medizinproduktemarktes auf kleine und mittlere Unternehmen, die etwa 40 Prozent des Gesamtumsatzes mit Medizinprodukten erwirtschaften. Da es sich bei diesen Unternehmen um Start-ups handelt, entscheiden sie sich dafür, die Prüfung von Medizinprodukten auszulagern, um Kosten zu senken und Zeit zu sparen. Daher wird der wachsende Bedarf in der Branche voraussichtlich das Wachstum des globalen Marktes für Prüfdienstleistungen für Medizinprodukte in den kommenden Jahren vorantreiben. Den Verbrauchern fortschrittliche Medizinproduktetechnologie zur Verfügung zu stellen, ist ein hohes
- Dieses KOSTENLOSE Beispiel umfasst eine Datenanalyse von Markttrends bis hin zu Schätzungen und Prognosen.
Risikoprojekt. Daher bieten die Unternehmen korrekte Tests an, indem sie genaue und zuverlässige Ergebnisse für die Prüfanforderungen für medizinische Geräte liefern, von kleinen Start-up-Unternehmen bis hin zu großen, etablierten Herstellern.
Zahlreiche Labore in Nordamerika, Europa und im asiatisch-pazifischen Raum verfügen über Kenntnisse zur Einhaltung gesetzlicher Vorschriften und qualifizierte GMP-/GLP-/ISO-17025-Tests, um schnelle Verbesserungszeiten durch den Einsatz des höchsten Serviceniveaus und der fortschrittlichsten Technologien für die mikrobiologischen, analytisch-chemischen, Biokompatibilitäts- und Verpackungstestanforderungen sicherzustellen.
In anderen Ländern gibt es verschiedene Regulierungsbehörden, die die Zulassung von Medizinprodukten regeln. In Spanien werden Medizinprodukte von der spanischen Agentur für Arzneimittel und Gesundheitsprodukte (AEMPS) kontrolliert und zugelassen. Das Lebensmittel- und Arzneimittelgesetz (FDA) legt einen regulatorischen Rahmen für zahlreiche Medizinprodukte fest. Das Medizinproduktebüro ist eine weitere Behörde, die für Richtlinien zu Medizinprodukten zuständig ist, die den Verkauf und Import von Medizinprodukten erlauben.
Für alle Medizinprodukte gelten exklusive und systematische Testanforderungen der FDA, der China Food and Drug Administration (CFDA), der EU-benannten Stellen und anderer Aufsichtsbehörden, die vor der Markteinführung befolgt werden sollten.
In Kanada hat Health Canada die Meldepflicht für Vorfälle mit Medizinprodukten durch Importeure und Hersteller eingeführt und regt auch medizinisches Personal, Krankenhäuser und Verbraucher/Patienten zur Meldung an. In Mexiko ist COFEPRIS für die Zulassung und Registrierung des Medizinprodukts zuständig. Der Hersteller muss alle Testanforderungen erfüllen und die COFEPRIS-Zulassung beantragen.
Die Medicines and Healthcare products Regulatory Agency (MHRA) ist die zuständige Behörde, die in Großbritannien die Gesetze zu Medizinprodukten durchsetzt. Sie prüft Medizinprodukte mit potenziellen Problemen und gewährleistet deren Sicherheit und Qualität. In Japan arbeiten das japanische Ministerium für Gesundheit, Arbeit und Soziales (MHLW) und die Pharmaceuticals and Medical Devices Agency (PMDA) zusammen, um wissenschaftliche Tests von Medizinprodukten durchzuführen, die zur Vermarktung zugelassen sind, um deren Sicherheit nach der Markteinführung zu überwachen.
Daher ist zu erwarten, dass die zunehmend strengeren Vorschriften für innovative und präzise Geräte das Wachstum des Marktes für Prüfdienstleistungen für medizinische Geräte im Prognosezeitraum vorantreiben werden.
Servicebasierte Einblicke
In Bezug auf die Dienstleistungen ist der Markt für Medizinprodukte-Testdienste im Gesundheitswesen in Biokompatibilitätstests, Chemietests, Mikrobiologie- und Sterilitätstests sowie Verpackungsvalidierung unterteilt. Im Jahr 2018 hatten die Mikrobiologie- und Sterilitätstests mit 53,55 % den größten Marktanteil am Markt für Medizinprodukte-Testdienste.
Regionale Einblicke in den Markt für Testdienste für medizinische Geräte
Die regionalen Trends und Faktoren, die den Markt für Testdienste für medizinische Geräte während des gesamten Prognosezeitraums beeinflussen, wurden von den Analysten von Insight Partners ausführlich erläutert. In diesem Abschnitt werden auch die Marktsegmente und die Geografie von Testdiensten für medizinische Geräte in Nordamerika, Europa, im asiatisch-pazifischen Raum, im Nahen Osten und Afrika sowie in Süd- und Mittelamerika erörtert.
- Erhalten Sie regionale Daten zum Markt für Prüfdienstleistungen für medizinische Geräte
Umfang des Marktberichts zu Prüfdienstleistungen für medizinische Geräte
| Berichtsattribut | Details |
|---|---|
| Marktgröße im Jahr 2018 | 5,51 Milliarden US-Dollar |
| Marktgröße bis 2027 | 14,66 Milliarden US-Dollar |
| Globale CAGR (2018 - 2027) | 11,7 % |
| Historische Daten | 2016-2017 |
| Prognosezeitraum | 2019–2027 |
| Abgedeckte Segmente | Nach Service
|
| Abgedeckte Regionen und Länder | Nordamerika
|
| Marktführer und wichtige Unternehmensprofile |
|
Marktteilnehmerdichte: Der Einfluss auf die Geschäftsdynamik
Der Markt für Testdienstleistungen für medizinische Geräte wächst rasant. Dies wird durch die steigende Nachfrage der Endnutzer aufgrund von Faktoren wie sich entwickelnden Verbraucherpräferenzen, technologischen Fortschritten und einem größeren Bewusstsein für die Vorteile des Produkts vorangetrieben. Mit der steigenden Nachfrage erweitern Unternehmen ihr Angebot, entwickeln Innovationen, um die Bedürfnisse der Verbraucher zu erfüllen, und nutzen neue Trends, was das Marktwachstum weiter ankurbelt.
Die Marktteilnehmerdichte bezieht sich auf die Verteilung der Firmen oder Unternehmen, die in einem bestimmten Markt oder einer bestimmten Branche tätig sind. Sie gibt an, wie viele Wettbewerber (Marktteilnehmer) in einem bestimmten Marktraum im Verhältnis zu seiner Größe oder seinem gesamten Marktwert präsent sind.
Die wichtigsten Unternehmen auf dem Markt für Prüfdienstleistungen für medizinische Geräte sind:
- SGS SA
- Eurofins
- Toxikon
- Pace Analytical Services, LLC
- Intertek Group plc
Haftungsausschluss : Die oben aufgeführten Unternehmen sind nicht in einer bestimmten Reihenfolge aufgeführt.
- Überblick über die wichtigsten Akteure auf dem Markt für Prüfdienstleistungen für medizinische Geräte
Phasenbasierte Erkenntnisse
Basierend auf den Phasen ist der Markt für Medizinprodukte-Testdienste im Gesundheitswesen in präklinische und klinische Bereiche unterteilt. Im Jahr 2018 hielt das präklinische Segment einen beträchtlichen Marktanteil von 68,17 % des Marktes für Medizinprodukte-Testdienste nach Phasen.
Die Akteure auf dem Markt für Prüfdienstleistungen für medizinische Geräte im Gesundheitswesen verfolgen Strategien zur Produkteinführung und -erweiterung, um den sich weltweit ändernden Kundenanforderungen gerecht zu werden und so ihren Markennamen weltweit zu wahren.
Prüfdienste für medizinische Geräte im Gesundheitsmarkt – nach Dienst
- Biokompatibilitätstest
- Chemietest
- Mikrobiologie und Sterilitätstests
- Paketvalidierung
Testdienste für medizinische Geräte im Gesundheitsmarkt – nach Phase
- Präklinisch
- Klinisch
Testdienste für medizinische Geräte im Gesundheitsmarkt – nach Geografie
Nordamerika
- UNS
- Kanada
- Mexiko
Europa
- Frankreich
- Deutschland
- Italien
- Vereinigtes Königreich
- Spanien
- Restliches Europa
Asien-Pazifik (APAC)
- China
- Indien
- Südkorea
- Japan
- Australien
- Restlicher Asien-Pazifik-Raum
Naher Osten und Afrika (MEA)
- Südafrika
- Saudi-Arabien
- Vereinigte Arabische Emirate
- Rest von MEA
Südamerika und Mittelamerika (SCAM)
- Brasilien
- Argentinien
- Rest von SCAM
Firmenprofile
- SGS SA
- Eurofins
- Toxikon
- Pace Analytical Services, LLC
- Intertek Group plc
- Gesellschaften, beginnend mit NORTH
- Charles-Fluss
- WuXi AppTec
- Element-Materialien-Technologie
- TÜV SÜD AG
- Historische Analyse (2 Jahre), Basisjahr, Prognose (7 Jahre) mit CAGR
- PEST- und SWOT-Analyse
- Marktgröße Wert/Volumen – Global, Regional, Land
- Branche und Wettbewerbsumfeld
- Excel-Datensatz

Report Coverage
Revenue forecast, Company Analysis, Industry landscape, Growth factors, and Trends
Segment Covered
This text is related
to segments covered.

Regional Scope
North America, Europe, Asia Pacific, Middle East & Africa, South & Central America
Country Scope
This text is related
to country scope.
Trends and growth analysis reports related to Life Sciences : READ MORE..
The List of Companies
- SGS SA
- Eurofins
- Toxikon
- Pace Analytical Services, LLC
- Intertek Group plc
- NORTH AMERICAN SCIENCE ASSOCIATES INC.
- Charles River
- WuXi AppTec
- Element Materials Technology
- TÜV SÜD AG
The Insight Partners performs research in 4 major stages: Data Collection & Secondary Research, Primary Research, Data Analysis and Data Triangulation & Final Review.
- Data Collection and Secondary Research:
As a market research and consulting firm operating from a decade, we have published and advised several client across the globe. First step for any study will start with an assessment of currently available data and insights from existing reports. Further, historical and current market information is collected from Investor Presentations, Annual Reports, SEC Filings, etc., and other information related to company’s performance and market positioning are gathered from Paid Databases (Factiva, Hoovers, and Reuters) and various other publications available in public domain.
Several associations trade associates, technical forums, institutes, societies and organization are accessed to gain technical as well as market related insights through their publications such as research papers, blogs and press releases related to the studies are referred to get cues about the market. Further, white papers, journals, magazines, and other news articles published in last 3 years are scrutinized and analyzed to understand the current market trends.
- Primary Research:
The primarily interview analysis comprise of data obtained from industry participants interview and answers to survey questions gathered by in-house primary team.
For primary research, interviews are conducted with industry experts/CEOs/Marketing Managers/VPs/Subject Matter Experts from both demand and supply side to get a 360-degree view of the market. The primary team conducts several interviews based on the complexity of the markets to understand the various market trends and dynamics which makes research more credible and precise.
A typical research interview fulfils the following functions:
- Provides first-hand information on the market size, market trends, growth trends, competitive landscape, and outlook
- Validates and strengthens in-house secondary research findings
- Develops the analysis team’s expertise and market understanding
Primary research involves email interactions and telephone interviews for each market, category, segment, and sub-segment across geographies. The participants who typically take part in such a process include, but are not limited to:
- Industry participants: VPs, business development managers, market intelligence managers and national sales managers
- Outside experts: Valuation experts, research analysts and key opinion leaders specializing in the electronics and semiconductor industry.
Below is the breakup of our primary respondents by company, designation, and region:
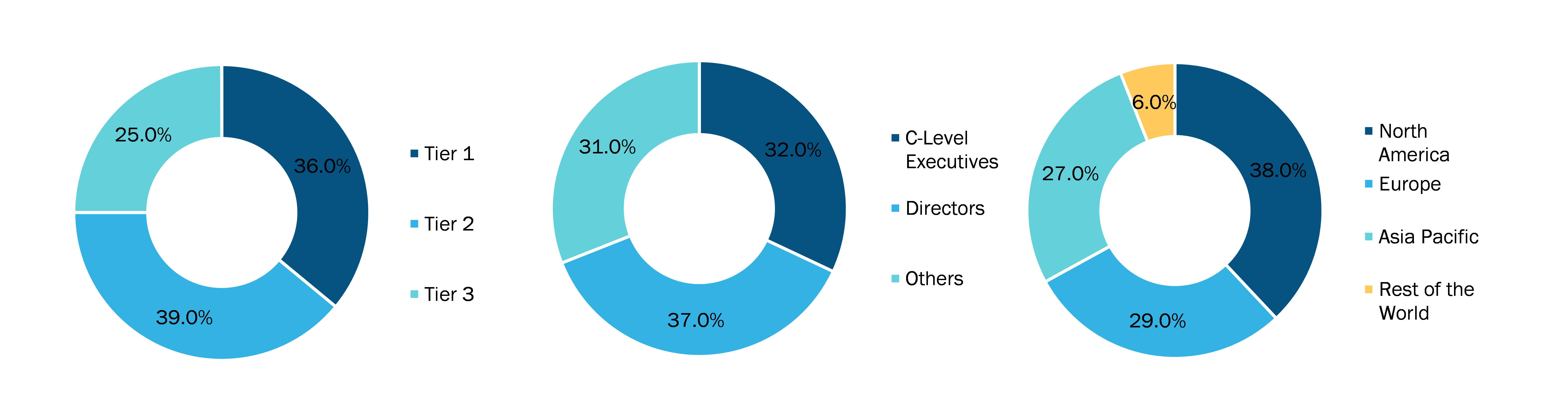
Once we receive the confirmation from primary research sources or primary respondents, we finalize the base year market estimation and forecast the data as per the macroeconomic and microeconomic factors assessed during data collection.
- Data Analysis:
Once data is validated through both secondary as well as primary respondents, we finalize the market estimations by hypothesis formulation and factor analysis at regional and country level.
- Macro-Economic Factor Analysis:
We analyse macroeconomic indicators such the gross domestic product (GDP), increase in the demand for goods and services across industries, technological advancement, regional economic growth, governmental policies, the influence of COVID-19, PEST analysis, and other aspects. This analysis aids in setting benchmarks for various nations/regions and approximating market splits. Additionally, the general trend of the aforementioned components aid in determining the market's development possibilities.
- Country Level Data:
Various factors that are especially aligned to the country are taken into account to determine the market size for a certain area and country, including the presence of vendors, such as headquarters and offices, the country's GDP, demand patterns, and industry growth. To comprehend the market dynamics for the nation, a number of growth variables, inhibitors, application areas, and current market trends are researched. The aforementioned elements aid in determining the country's overall market's growth potential.
- Company Profile:
The “Table of Contents” is formulated by listing and analyzing more than 25 - 30 companies operating in the market ecosystem across geographies. However, we profile only 10 companies as a standard practice in our syndicate reports. These 10 companies comprise leading, emerging, and regional players. Nonetheless, our analysis is not restricted to the 10 listed companies, we also analyze other companies present in the market to develop a holistic view and understand the prevailing trends. The “Company Profiles” section in the report covers key facts, business description, products & services, financial information, SWOT analysis, and key developments. The financial information presented is extracted from the annual reports and official documents of the publicly listed companies. Upon collecting the information for the sections of respective companies, we verify them via various primary sources and then compile the data in respective company profiles. The company level information helps us in deriving the base number as well as in forecasting the market size.
- Developing Base Number:
Aggregation of sales statistics (2020-2022) and macro-economic factor, and other secondary and primary research insights are utilized to arrive at base number and related market shares for 2022. The data gaps are identified in this step and relevant market data is analyzed, collected from paid primary interviews or databases. On finalizing the base year market size, forecasts are developed on the basis of macro-economic, industry and market growth factors and company level analysis.
- Data Triangulation and Final Review:
The market findings and base year market size calculations are validated from supply as well as demand side. Demand side validations are based on macro-economic factor analysis and benchmarks for respective regions and countries. In case of supply side validations, revenues of major companies are estimated (in case not available) based on industry benchmark, approximate number of employees, product portfolio, and primary interviews revenues are gathered. Further revenue from target product/service segment is assessed to avoid overshooting of market statistics. In case of heavy deviations between supply and demand side values, all thes steps are repeated to achieve synchronization.
We follow an iterative model, wherein we share our research findings with Subject Matter Experts (SME’s) and Key Opinion Leaders (KOLs) until consensus view of the market is not formulated – this model negates any drastic deviation in the opinions of experts. Only validated and universally acceptable research findings are quoted in our reports.
We have important check points that we use to validate our research findings – which we call – data triangulation, where we validate the information, we generate from secondary sources with primary interviews and then we re-validate with our internal data bases and Subject matter experts. This comprehensive model enables us to deliver high quality, reliable data in shortest possible time.

 Holen Sie sich ein kostenloses Muster für diesen Bericht
Holen Sie sich ein kostenloses Muster für diesen Bericht