El tamaño del mercado de software de farmacovigilancia y seguridad de medicamentos en Europa se valoró en 52,37 millones de dólares estadounidenses en 2023 y se espera que alcance los 84,66 millones de dólares estadounidenses en 2031; se estima que registrará una CAGR del 6,2 % durante 2023-2031. Es probable que el software de farmacovigilancia y seguridad de medicamentos basado en la nube traiga nuevas tendencias clave al mercado en los próximos años.
Análisis del mercado europeo de software de farmacovigilancia y seguridad de medicamentos
El software de farmacovigilancia y seguridad de medicamentos garantiza una detección y evaluación rápidas de las reacciones adversas asociadas a los medicamentos. Al mejorar la supervisión de la seguridad y automatizar la recopilación y el análisis de datos, el software acelera la identificación de posibles problemas de seguridad, lo que permite una intervención rápida para mitigar los riesgos. Este enfoque proactivo mejora el cumplimiento normativo, la seguridad del paciente y los resultados generales de salud pública. Además, con la presencia de análisis avanzados y capacidades de monitoreo en tiempo real, el software de farmacovigilancia y seguridad de medicamentos proporciona un marco sólido para optimizar la vigilancia de la seguridad de los medicamentos. La integración de la IA y el análisis predictivo con el software de farmacovigilancia y seguridad de medicamentos mejora la capacidad de identificar posibles riesgos de seguridad antes de que se conviertan en problemas graves. Estas tecnologías avanzadas ayudan a analizar grandes volúmenes de datos estructurados y no estructurados para detectar señales y tendencias de seguridad futuras, lo que desencadena estrategias proactivas de mitigación de riesgos. Por lo tanto, debido a varias ventajas, la demanda de software de farmacovigilancia y seguridad de medicamentos está aumentando en Europa.
Panorama del mercado europeo de software de farmacovigilancia y seguridad de medicamentos
La farmacovigilancia es la ciencia que mantiene la salud pública garantizando la seguridad y eficacia de los productos farmacéuticos. El software de farmacovigilancia y seguridad de los medicamentos es una herramienta vital que aborda los errores de entrada manual de datos, el abrumador volumen de datos de seguridad y varios otros desafíos. Desde is the science of maintaining public health by ensuring the safety and efficacy of pharmaceutical products. los ensayos clínicos hasta la vigilancia posterior a la comercialización, este software es indispensable durante todo el ciclo de vida del desarrollo de medicamentos. El software de farmacovigilancia y seguridad de medicamentos ayuda a reducir el tiempo de procesamiento de eventos adversos, así como a mejorar la seguridad del paciente mediante la detección temprana de señales. A medida que evolucionan las regulaciones y se intensifica la colaboración europea, la adopción de software de farmacovigilancia y seguridad de medicamentos es ventajosa, lo que la hace imperativa para las empresas farmacéuticas y los organismos reguladores. En 2022, el Esquema de cooperación en materia de inspección farmacéutica (PIC/S) actualizó sus directrices sobre farmacovigilancia para cumplir con los estándares internacionales, destacando la importancia de un software sólido de farmacovigilancia y seguridad de medicamentos. Además, el software garantiza el cumplimiento de los estándares regulatorios al facilitar la creación de informes de seguridad completos y las presentaciones a las autoridades reguladoras, lo que ayuda a las empresas a evitar sanciones y mantener su reputación.Pharmacovigilance and drug safety software is a vital tool that addresses manual data entry errors, the overwhelming volume of safety data, and various other challenges. From lifecycle. Pharmacovigilance and drug safety software helps reduce adverse event processing time as well as improve patient safety through early signal detection. As regulations evolve and European collaboration intensifies, the adoption of pharmacovigilance and drug safety software is advantageous, making it imperative for pharmaceutical companies and regulatory bodies. In 2022, The Pharmaceutical Inspection Co-operation Scheme (PIC/S) updated its guidelines on pharmacovigilance to adhere to international standards, highlighting the importance of robust pharmacovigilance and drug safety software. Further, the software ensures compliance with regulatory standards by facilitating the creation of comprehensive safety reports and submissions to regulatory authorities, which helps companies avoid penalties and maintain their reputation.
Personalice la investigación para adaptarla a sus necesidades
Podemos optimizar y adaptar el análisis y el alcance que no se alcanzan con nuestras ofertas estándar. Esta flexibilidad le ayudará a obtener la información exacta que necesita para la planificación y la toma de decisiones de su negocio.
Mercado europeo de software de farmacovigilancia y seguridad de medicamentos: perspectivas estratégicasPharmacovigilance and Drug Safety Software Market:
Tasa de crecimiento anual compuesta (2023-2031)6,2%- Tamaño del mercado 2023
US$ 52,37 millones - Tamaño del mercado 2031
US$ 84,66 millones

Dinámica del mercado
- Aumento de la incidencia de reacciones adversas a medicamentos
- Globalización de la farmacovigilanciaPharmacovigilance
- Aumento de las tasas de desarrollo de fármacos
- Farmacovigilancia basada en la nube
- Software de seguridad de medicamentos
- Integración de software con IA y ML
- PNL
Actores clave
- Aris Europa
- ICON plc Syneos Salud
- Accenture
- IQVIA
- Pacto Genético
- Competente
- Corporación Paraxel Internacional
- Corporación de laboratorio de América Holdings
- Aplicación máxima
- Tecnologías Clinevo
Panorama regional
- Europa
Segmentación del mercado
 Ofrenda
Ofrenda- Software
- Servicios
 Despliegue
Despliegue- Nube
- En las instalaciones
 Tamaño de la empresa
Tamaño de la empresa- Grandes empresas
- PYMES
 Forma
Forma- Estándar
- Personalizado
- El PDF de muestra muestra la estructura del contenido y la naturaleza de la información con análisis cualitativo y cuantitativo.
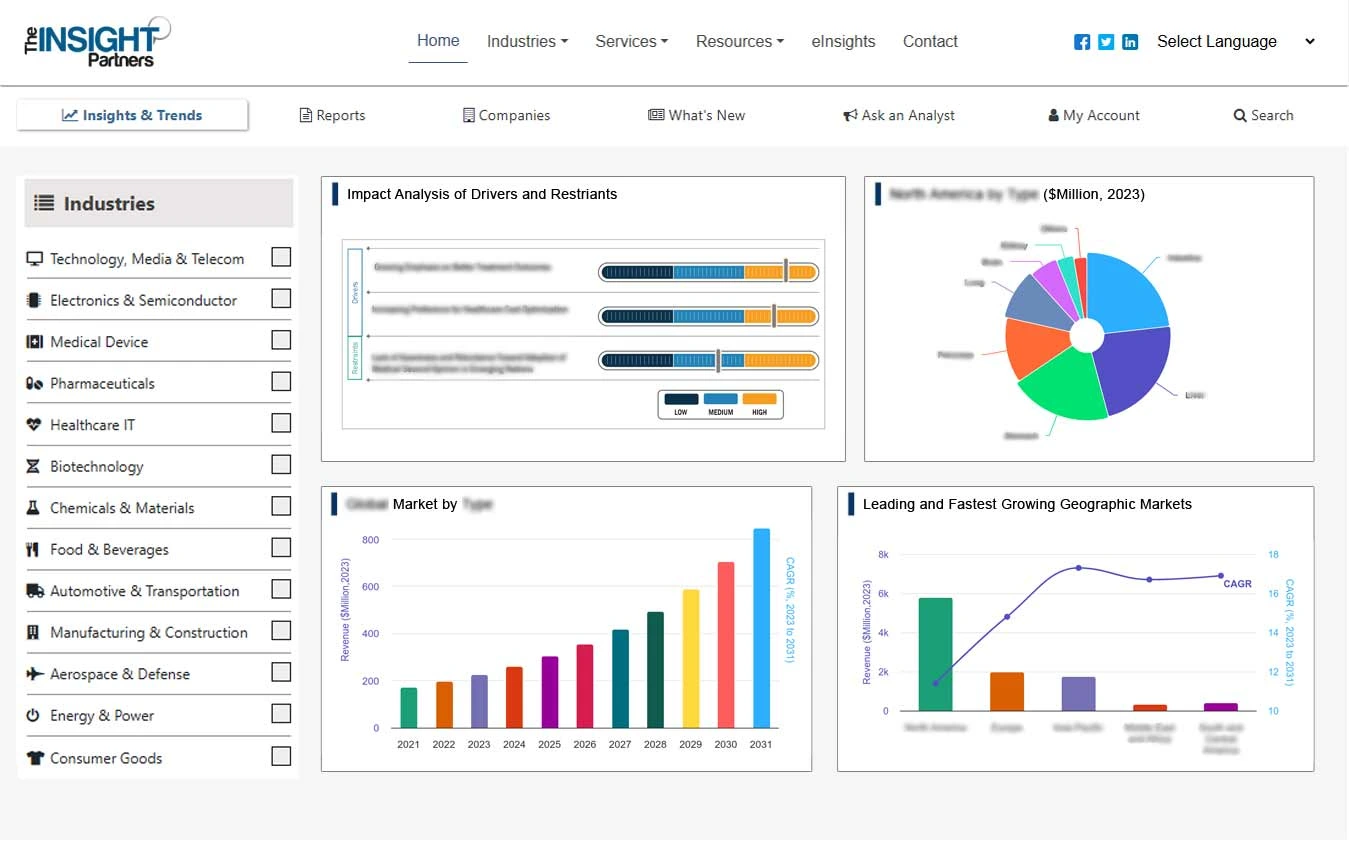
Factores impulsores y oportunidades del mercado europeo de software de farmacovigilancia y seguridad de medicamentos
Aumento de la incidencia de reacciones adversas a medicamentos
En Europa, las reacciones adversas a medicamentos (RAM) pueden ser una causa importante de muerte y enfermedad. Como todos los medicamentos tienen el potencial de provocar reacciones adversas, es necesario realizar un análisis de riesgo-beneficio siempre que se prescribe un medicamento. Las RAM siguen siendo un desafío en la atención médica moderna, en particular dada la creciente complejidad de las terapias, el envejecimiento de la población y el aumento de la multimorbilidad en Europa. El software de farmacovigilancia permite a los proveedores de atención médica y a las compañías farmacéuticas recopilar, analizar e informar sistemáticamente datos relacionados con las RAM y superar los desafíos asociados con ellas.
Las reacciones adversas a medicamentos son una de las principales causas del aumento de las tasas de mortalidad en Europa. Según el informe de la Agencia Europea de Medicamentos (EUDA), en términos de sobredosis, la tasa de mortalidad en la Unión Europea en 2021 fue de aproximadamente 18,3 muertes por millón de habitantes de entre 15 y 64 años. Además, en 2021 se produjeron en la Unión Europea al menos 6166 muertes causadas por sobredosis de drogas ilícitas (5796 en 2020). Este total alcanzó las 6677 muertes si se incluyen Noruega y Turquía (6434 en 2020).
A medida que se notifican y reconocen más reacciones adversas a medicamentos, las compañías farmacéuticas , los proveedores de atención médica y los organismos reguladores enfrentan una mayor presión para mejorar los procesos de monitoreo y notificación de la seguridad de los medicamentos. Esto requiere la adopción de software de farmacovigilancia y seguridad de medicamentos para recopilar, analizar y gestionar el creciente volumen de datos de seguridad. Este software ayuda a agilizar el proceso de detección, evaluación y prevención de efectos adversos, lo que permite tiempos de respuesta más rápidos y evaluaciones de riesgos más precisas. Por lo tanto, la creciente incidencia de reacciones adversas a medicamentos impulsa el crecimiento del mercado europeo de software de farmacovigilancia y seguridad de medicamentos .
Integración de software con IA, ML y PNL
La inteligencia artificial (IA), el aprendizaje automático (AA), el procesamiento del lenguaje natural (PLN) y otras tecnologías están transformando las cargas de trabajo de farmacovigilancia que consumen muchos recursos, garantizando un enfoque más informado y más eficiente. Las plataformas de software de farmacovigilancia y seguridad de medicamentos están equipadas en su mayoría con análisis avanzados y capacidades de IA que mejoran la detección de señales de seguridad. Estas herramientas pueden analizar grandes cantidades de datos, identificando correlaciones y patrones que los métodos tradicionales podrían pasar por alto. El análisis predictivo impulsado por IA también puede predecir posibles problemas de seguridad, lo que permite a las empresas tomar medidas proactivas. Los modelos de AA se aprovechan para predecir posibles eventos adversos asociados con el consumo de medicamentos. Por ejemplo, las campañas de farmacovigilancia utilizan el AA para examinar grandes conjuntos de datos, detectando patrones que podrían indicar un riesgo de reacciones adversas a los medicamentos. Los algoritmos de AA son particularmente hábiles para manejar datos no estructurados, como las redes sociales y los registros de pacientes, para predecir problemas de seguridad.
Los sistemas de IA se están utilizando progresivamente para avanzar en el control de la seguridad de los medicamentos en tiempo real. Esta vigilancia proactiva incluye datos de ensayos clínicos, escaneo de literatura médica y registros de pacientes para eventos adversos (EA); también puede mejorar la precisión y velocidad de las detecciones de ADR. Además, utilizando NLP, los sistemas de IA pueden extraer información relevante, como nombres de medicamentos y síntomas, de vastos conjuntos de datos textuales, lo que permite informar eventos adversos de manera precisa y rápida. Esto acelera la identificación de problemas de seguridad de medicamentos desconocidos o nuevos, mejorando así significativamente los avances en los esfuerzos de farmacovigilancia. Varias empresas ofrecen software de farmacovigilancia y seguridad de medicamentos basado en IA, incluida ArisGlobal. Por lo tanto, se espera que la integración de software de farmacovigilancia y seguridad de medicamentos con IA, ML y NLP cree oportunidades lucrativas para el crecimiento del mercado durante el período de pronóstico.
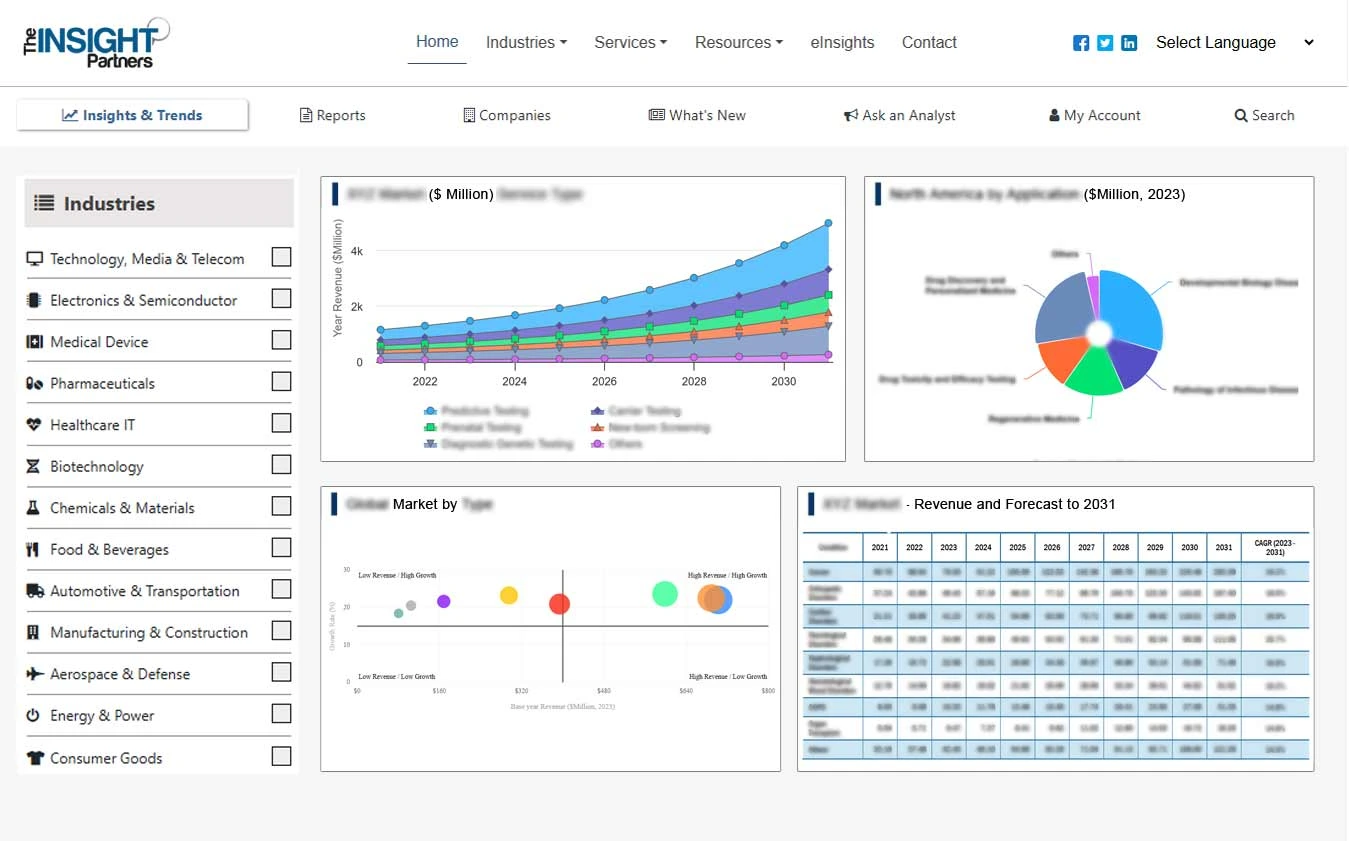
Informe de mercado de software de farmacovigilancia y seguridad de medicamentos de Europa: análisis de segmentación
Los segmentos clave que contribuyeron a la derivación del análisis del mercado de software de farmacovigilancia y seguridad de medicamentos de Europa son las ofertas, el tamaño de la organización, la implementación, la forma, la funcionalidad y el usuario final.
- Según el tamaño de las organizaciones, el mercado europeo de software de farmacovigilancia y seguridad de medicamentos se divide en grandes empresas y pymes. El segmento de las grandes empresas dominó el mercado en 2023.
- En cuanto a la oferta, el mercado se divide en software y servicios. El segmento de software tuvo una mayor participación en el mercado en 2023.
- Según la implementación, el mercado europeo de software de farmacovigilancia y seguridad de medicamentos se divide en nube y local. El segmento de la nube dominó el mercado en 2023
- Según la forma, el mercado europeo de software de farmacovigilancia y seguridad de medicamentos se divide en estándar y personalizado. El segmento estándar dominó el mercado en 2023.
- Por funcionalidad, el mercado europeo de software de farmacovigilancia y seguridad de medicamentos se segmenta en gestión de casos, gestión de señales y riesgos, calidad y cumplimiento, soporte de auditoría y cumplimiento de la formación, seguimiento de problemas y seguimiento de eventos adversos, gestión de seguridad clínica y seguridad de ensayos clínicos, redacción médica, análisis de atención sanitaria y otros. El segmento de gestión de señales y riesgos tuvo la mayor participación del mercado en 2023.
- Según el usuario final, el mercado europeo de software de farmacovigilancia y seguridad de medicamentos está segmentado en empresas farmacéuticas y biotecnológicas, organizaciones de investigación por contrato, empresas de subcontratación de procesos comerciales y otros proveedores de servicios de farmacovigilancia. El segmento de empresas farmacéuticas y biotecnológicas dominó el mercado en 2023.
Análisis de la cuota de mercado del software de farmacovigilancia y seguridad de medicamentos en Europa por geografía
El mercado europeo de software de farmacovigilancia y seguridad de medicamentos está segmentado en Francia, Alemania, Italia, España, el Reino Unido y el resto de Europa. La creciente demanda de software de farmacovigilancia y seguridad de medicamentos en Europa se atribuye a varios factores, incluidos los requisitos regulatorios, el aumento de las aprobaciones de medicamentos, el creciente énfasis en la seguridad del paciente y los avances en la tecnología. El sistema de farmacovigilancia de la UE es uno de los más avanzados del mundo. La Agencia Europea de Medicamentos (EMA) y otros organismos reguladores están imponiendo estrictos requisitos de farmacovigilancia que requieren la adopción de soluciones de software avanzadas. Por ejemplo, la introducción de la Directiva de farmacovigilancia de la UE (2010/84/UE) y el posterior Reglamento (UE) n.º 1235/2010 han impuesto reglas más estrictas para el monitoreo de reacciones adversas a medicamentos (RAM). Las empresas deben informar los datos de seguridad en tiempo real, lo que aumenta significativamente la demanda de sistemas de software eficientes capaces de manejar grandes volúmenes de datos.
Alcance del informe sobre el mercado de software de farmacovigilancia y seguridad de medicamentos en Europa
| Atributo del informe | Detalles |
|---|---|
| Tamaño del mercado en 2023 | US$ 52,37 millones |
| Tamaño del mercado en 2031 | US$ 84,66 millones |
| Tasa de crecimiento anual compuesta (CAGR) global (2023-2031) | 6,2% |
| Datos históricos | 2021-2022 |
| Período de pronóstico | 2024-2031 |
| Segmentos cubiertos | Al ofrecer
|
| Regiones y países cubiertos | Europa
|
| Líderes del mercado y perfiles de empresas clave |
|
- El PDF de muestra muestra la estructura del contenido y la naturaleza de la información con análisis cualitativo y cuantitativo.
Noticias y desarrollos recientes del mercado europeo de software de farmacovigilancia y seguridad de medicamentos
El mercado europeo de software de farmacovigilancia y seguridad de medicamentos se evalúa mediante la recopilación de datos cualitativos y cuantitativos a partir de una investigación primaria y secundaria, que incluye importantes publicaciones corporativas, datos de asociaciones y bases de datos. A continuación se enumeran algunos de los desarrollos clave en el mercado europeo de software de farmacovigilancia y seguridad de medicamentos:
- ArisGlobal, líder del mercado en soluciones tecnológicas para el desarrollo de fármacos a nivel mundial, anunció que Medac, un fabricante farmacéutico con sede en Alemania especializado en los campos de la oncología y la hematología, la urología y las enfermedades autoinmunes, eligió LifeSphere Safety para modernizar sus procesos de seguridad de los fármacos. El análisis preciso y específico de cada paciente y población es fundamental para minimizar los riesgos del tratamiento para los pacientes, lo que favorece el mejor resultado posible del tratamiento. (Fuente: ArisGlobal, comunicado de prensa, mayo de 2023)
- IQVIA, un proveedor líder mundial de análisis avanzados, soluciones tecnológicas y servicios de investigación clínica para la industria de las ciencias biológicas, anunció una colaboración estratégica con Argenx para avanzar en el tratamiento de pacientes que padecen enfermedades autoinmunes raras a través de servicios y soluciones de seguridad de farmacovigilancia (PV) innovadores e integrados basados en tecnología. (Fuente: IQVIA, comunicado de prensa, enero de 2023)
Informe sobre el mercado europeo de software de farmacovigilancia y seguridad de medicamentos: cobertura y resultados
El informe "Tamaño y pronóstico del mercado de software de farmacovigilancia y seguridad de medicamentos en Europa (2021-2031)" proporciona un análisis detallado del mercado que cubre las áreas mencionadas a continuación:
- Tamaño del mercado europeo de software de farmacovigilancia y seguridad de medicamentos y pronóstico a nivel de país para todos los segmentos clave del mercado cubiertos por el alcance
- Tendencias del mercado europeo de software de farmacovigilancia y seguridad de medicamentos, así como dinámicas del mercado, como impulsores, restricciones y oportunidades clave
- Análisis PEST y FODA detallados
- Análisis del mercado europeo de software de farmacovigilancia y seguridad de medicamentos que abarca las tendencias clave del mercado, el marco regional, los principales actores, las regulaciones y los desarrollos recientes del mercado
- Análisis del panorama de la industria y de la competencia que abarca la concentración del mercado, el análisis de mapas de calor, los actores destacados y los desarrollos recientes para el mercado europeo de software de farmacovigilancia y seguridad de medicamentos
- Perfiles detallados de empresas
- Análisis histórico (2 años), año base, pronóstico (7 años) con CAGR
- Análisis PEST y FODA
- Tamaño del mercado Valor/volumen: global, regional, nacional
- Industria y panorama competitivo
- Conjunto de datos de Excel

Report Coverage
Revenue forecast, Company Analysis, Industry landscape, Growth factors, and Trends
Segment Covered
This text is related
to segments covered.

Regional Scope
North America, Europe, Asia Pacific, Middle East & Africa, South & Central America
Country Scope
This text is related
to country scope.
Preguntas frecuentes
The Europe pharmacovigilance and drug safety software market was estimated to be US$ 52.37 million in 2023 and is expected to grow at a CAGR of 6.2% during the forecast period 2023 - 2031.
Cloud-based pharmacovigilance and drug safety software, which is anticipated to play a significant role in the Europe pharmacovigilance and drug safety software market in the coming years.
Rise in incidences of adverse drug reactions, globalization of pharmacovigilance, surge in drug development rates are the major factors that propel the Europe pharmacovigilance and drug safety software market.
The key players holding majority shares in the Europe pharmacovigilance and drug safety software market are ArisEurope, ICON plc, Syneos Health, Accenture, IQVIA, Genpact, Cognizant, Paraxel International Corporation, Laboratory Corporation of America Holdings, Max Application, Clinevo Technologies, Qinecsa Solutions, AB Cube, and Veeva Systems.
The incremental growth expected to be recorded for the Europe pharmacovigilance and drug safety software market during the forecast period is US$ 32.29 million.
The Europe pharmacovigilance and drug safety software market is expected to reach US$ 84.66 million by 2031.
Trends and growth analysis reports related to Technology, Media and Telecommunications : READ MORE..
The List of Companies - Europe Pharmacovigilance and Drug Safety Software Market
- ArisGlobal LLC
- Max Application
- Oracle Corp
- Veeva Systems Inc
- IQVIA Holdings Inc
- ICON Plc
- Cognizant Technology Solutions Corp
- Accenture Plc
- Syneos Health Inc
- Genpact Ltd.
- AB Cube S.A.S.
- Laboratory Corp of America Holdings
- Parexel International Corp
- Qinecsa Solutions
- Clinevo Technologies
The Insight Partners performs research in 4 major stages: Data Collection & Secondary Research, Primary Research, Data Analysis and Data Triangulation & Final Review.
- Data Collection and Secondary Research:
As a market research and consulting firm operating from a decade, we have published and advised several client across the globe. First step for any study will start with an assessment of currently available data and insights from existing reports. Further, historical and current market information is collected from Investor Presentations, Annual Reports, SEC Filings, etc., and other information related to company’s performance and market positioning are gathered from Paid Databases (Factiva, Hoovers, and Reuters) and various other publications available in public domain.
Several associations trade associates, technical forums, institutes, societies and organization are accessed to gain technical as well as market related insights through their publications such as research papers, blogs and press releases related to the studies are referred to get cues about the market. Further, white papers, journals, magazines, and other news articles published in last 3 years are scrutinized and analyzed to understand the current market trends.
- Primary Research:
The primarily interview analysis comprise of data obtained from industry participants interview and answers to survey questions gathered by in-house primary team.
For primary research, interviews are conducted with industry experts/CEOs/Marketing Managers/VPs/Subject Matter Experts from both demand and supply side to get a 360-degree view of the market. The primary team conducts several interviews based on the complexity of the markets to understand the various market trends and dynamics which makes research more credible and precise.
A typical research interview fulfils the following functions:
- Provides first-hand information on the market size, market trends, growth trends, competitive landscape, and outlook
- Validates and strengthens in-house secondary research findings
- Develops the analysis team’s expertise and market understanding
Primary research involves email interactions and telephone interviews for each market, category, segment, and sub-segment across geographies. The participants who typically take part in such a process include, but are not limited to:
- Industry participants: VPs, business development managers, market intelligence managers and national sales managers
- Outside experts: Valuation experts, research analysts and key opinion leaders specializing in the electronics and semiconductor industry.
Below is the breakup of our primary respondents by company, designation, and region:
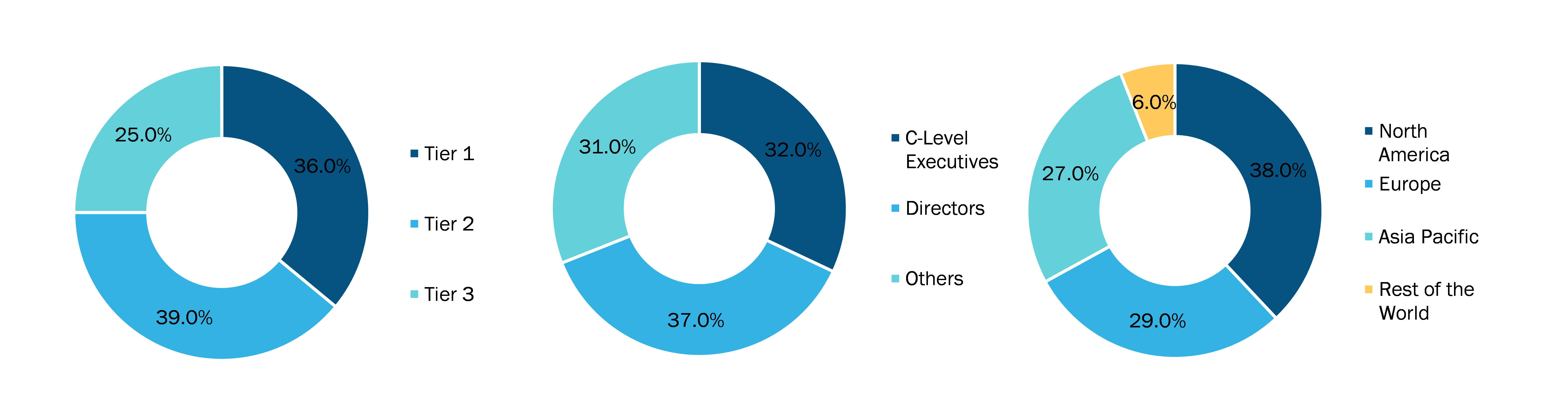
Once we receive the confirmation from primary research sources or primary respondents, we finalize the base year market estimation and forecast the data as per the macroeconomic and microeconomic factors assessed during data collection.
- Data Analysis:
Once data is validated through both secondary as well as primary respondents, we finalize the market estimations by hypothesis formulation and factor analysis at regional and country level.
- Macro-Economic Factor Analysis:
We analyse macroeconomic indicators such the gross domestic product (GDP), increase in the demand for goods and services across industries, technological advancement, regional economic growth, governmental policies, the influence of COVID-19, PEST analysis, and other aspects. This analysis aids in setting benchmarks for various nations/regions and approximating market splits. Additionally, the general trend of the aforementioned components aid in determining the market's development possibilities.
- Country Level Data:
Various factors that are especially aligned to the country are taken into account to determine the market size for a certain area and country, including the presence of vendors, such as headquarters and offices, the country's GDP, demand patterns, and industry growth. To comprehend the market dynamics for the nation, a number of growth variables, inhibitors, application areas, and current market trends are researched. The aforementioned elements aid in determining the country's overall market's growth potential.
- Company Profile:
The “Table of Contents” is formulated by listing and analyzing more than 25 - 30 companies operating in the market ecosystem across geographies. However, we profile only 10 companies as a standard practice in our syndicate reports. These 10 companies comprise leading, emerging, and regional players. Nonetheless, our analysis is not restricted to the 10 listed companies, we also analyze other companies present in the market to develop a holistic view and understand the prevailing trends. The “Company Profiles” section in the report covers key facts, business description, products & services, financial information, SWOT analysis, and key developments. The financial information presented is extracted from the annual reports and official documents of the publicly listed companies. Upon collecting the information for the sections of respective companies, we verify them via various primary sources and then compile the data in respective company profiles. The company level information helps us in deriving the base number as well as in forecasting the market size.
- Developing Base Number:
Aggregation of sales statistics (2020-2022) and macro-economic factor, and other secondary and primary research insights are utilized to arrive at base number and related market shares for 2022. The data gaps are identified in this step and relevant market data is analyzed, collected from paid primary interviews or databases. On finalizing the base year market size, forecasts are developed on the basis of macro-economic, industry and market growth factors and company level analysis.
- Data Triangulation and Final Review:
The market findings and base year market size calculations are validated from supply as well as demand side. Demand side validations are based on macro-economic factor analysis and benchmarks for respective regions and countries. In case of supply side validations, revenues of major companies are estimated (in case not available) based on industry benchmark, approximate number of employees, product portfolio, and primary interviews revenues are gathered. Further revenue from target product/service segment is assessed to avoid overshooting of market statistics. In case of heavy deviations between supply and demand side values, all thes steps are repeated to achieve synchronization.
We follow an iterative model, wherein we share our research findings with Subject Matter Experts (SME’s) and Key Opinion Leaders (KOLs) until consensus view of the market is not formulated – this model negates any drastic deviation in the opinions of experts. Only validated and universally acceptable research findings are quoted in our reports.
We have important check points that we use to validate our research findings – which we call – data triangulation, where we validate the information, we generate from secondary sources with primary interviews and then we re-validate with our internal data bases and Subject matter experts. This comprehensive model enables us to deliver high quality, reliable data in shortest possible time.
 Obtenga una muestra gratuita de este informe
Obtenga una muestra gratuita de este informe