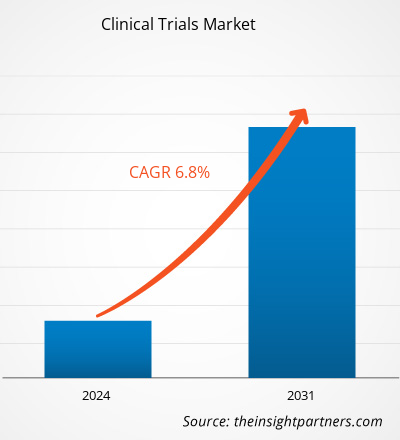
Le marché des essais cliniques devrait atteindre 73,33 milliards USD d'ici 2031, contre 43,37 milliards USD en 2023. Le marché devrait enregistrer un TCAC de 6,8 % au cours de la période 2023-2031. Les essais cliniques pilotés par l'IA devraient constituer une tendance future du marché dans les années à venir.
Analyse du marché des essais cliniques
Le marché des essais cliniques est principalement porté par les efforts continus déployés par les sociétés pharmaceutiques, biotechnologiques et de dispositifs médicaux pour innover en matière de produits. Parmi les autres facteurs contribuant à la progression du marché figurent la mondialisation des essais cliniques, les avancées rapides dans les technologies associées et une augmentation de la demande de CRO pour mener des essais cliniques. En outre, des conférences telles que « Global Clinical Trials Connect 2022 » offrent aux entreprises de ce marché une plate-forme pour se familiariser avec les avancées des essais cliniques et de la recherche clinique.
Aperçu du marché des essais cliniques
Les initiatives stratégiques croissantes des entreprises telles que les lancements de produits, les fusions et acquisitions, les partenariats et les expansions géographiques profitent au marché des essais cliniques . En septembre 2023, ICON plc a lancé sa solution de tokenisation d'essais cliniques de nouvelle génération. En combinant son moteur de tokenisation propriétaire, son accès à des données du monde réel et son expertise avancée en analyse clinique, ICON propose désormais un modèle opérationnel cohérent et transparent, fournissant des informations précieuses et à long terme sur la sécurité et l'efficacité des médicaments tout au long du cycle de vie du développement du produit. En février 2023, Labcorp a annoncé son intention de créer une nouvelle société, Fortrea, à la suite de la scission prévue de son activité de développement clinique. Une fois la scission de Labcorp achevée, Fortrea fonctionnera comme une CRO mondiale indépendante cotée en bourse pour offrir des services complets de développement de médicaments et de dispositifs médicaux.
Personnalisez ce rapport en fonction de vos besoins
Vous bénéficierez d'une personnalisation gratuite de n'importe quel rapport, y compris de certaines parties de ce rapport, d'une analyse au niveau des pays, d'un pack de données Excel, ainsi que de superbes offres et réductions pour les start-ups et les universités.
- Obtenez les principales tendances clés du marché de ce rapport.Cet échantillon GRATUIT comprendra une analyse de données, allant des tendances du marché aux estimations et prévisions.
Moteurs et opportunités du marché des essais cliniques
La pratique de l'externalisation des études cliniques avec une augmentation massive du nombre d'essais alimente le marché
Les essais cliniques sont menés pour déterminer si une nouvelle forme de produit médical, c'est-à-dire un médicament, un régime alimentaire ou un dispositif médical, est sûre et efficace. Les essais font principalement partie du processus global de développement de médicaments. Selon la National Library of Medicine (NLM), environ 52 000 nouvelles études ont été enregistrées auprès de la NLM (ClinicalTrials.gov) en 2020, et ce nombre est passé à environ 58 000 en 2023. En janvier 2023, la NLM a signalé 38 837 essais cliniques actifs aux États-Unis et 105 172 essais actifs dans le monde. Selon l'Agence européenne des médicaments, dans l'Union européenne (UE), environ 4 000 essais cliniques sont autorisés chaque année, dont environ 60 % sont associés à l'industrie pharmaceutique. L'augmentation du nombre d'essais cliniques peut être attribuée à la prévalence croissante des maladies chroniques dans le monde, ce qui crée une immense demande de traitements plus efficaces.
La complexité croissante des essais cliniques ajoute à l'importance cruciale de la bonne exécution et de la supervision des opérations menées dans les organisations de recherche. Pour éviter les erreurs dues à une mauvaise exécution, de nombreuses organisations de recherche sous-traitent les essais cliniques à des organisations de recherche clinique (CRO). Les CRO contribuent à la mise en œuvre réussie des essais cliniques grâce aux services qu'elles offrent à partir de leurs installations de haute qualité et de leur expertise approfondie en la matière. Elles sont progressivement devenues l'épine dorsale de l'industrie des essais cliniques grâce à leurs opérations efficaces et rentables qui profitent aux promoteurs d'essais. Selon un blog publié par Thermo Fisher Scientific, en 2022, les CRO ont exécuté environ 3 essais cliniques sur 4 pour rassurer les programmes cliniques des développeurs de médicaments, fournir une richesse d'expertise, accroître l'efficacité des temps et des coûts et fournir des données personnalisées et de haute qualité. Ainsi, le nombre croissant d'essais cliniques et la pratique de l'externalisation des essais à des CRO pour accroître la rentabilité et réduire les erreurs sont les principaux facteurs à l'origine de la croissance du marché des essais cliniques.
L'adoption d'essais cliniques décentralisés et d'essais cliniques hybrides offrira des opportunités de marché
Les sujets inscrits à des essais cliniques décentralisés (DCT) n’ont pas besoin d’accéder fréquemment aux sites d’essais en milieu hospitalier. Dans les DCT, les technologies numériques sont utilisées pour permettre la collecte et le suivi des données à distance, ainsi que pour rationaliser les communications entre les chercheurs et les participants. Une approche d’essai clinique hybride combine des activités à domicile et sur site, offrant la meilleure expérience patient et répondant à des régimes de protocole complexes, gagnant du terrain dans divers domaines thérapeutiques et parcours de phase d’essai. Des défis tels que la confidentialité des patients, la sécurité des données, les barrières réglementaires et les régimes de protocole complexes ont entravé l’adoption des DCT dans le passé. Cependant, la pandémie de COVID-19 a contraint les promoteurs d’essais cliniques à adopter des techniques cliniques décentralisées et hybrides pour développer des médicaments, car les études en personne n’étaient pas réalisables dans le contexte de la crise sanitaire . Avec les restrictions imposées sur les déplacements, la seule façon de collecter des données et de poursuivre les essais était de travailler à distance et d’utiliser de manière optimale les technologies pour accélérer les processus. Selon les données fournies par McKinsey, environ 70 % des participants potentiels aux essais cliniques résident loin des sites d’essai. Par conséquent, la décentralisation élargit l’accès aux essais pour atteindre un nombre plus important de sujets, constitué potentiellement d’un bassin de patients plus diversifié. Les essais cliniques hybrides permettent aux sponsors d’intégrer stratégiquement des éléments DCT dans les plans d’étude. Ces modèles d’essai offrent une flexibilité sans précédent ; ainsi, de plus en plus d’entreprises manifestent leur intérêt pour les essais hybrides, ce qui redéfinit le paysage de l’industrie. Selon ObvioHealth, la FDA avait prévu de dévoiler des protocoles pour soutenir l’utilisation des méthodes DCT en 2023 afin d’améliorer la crédibilité de la recherche clinique future. Ainsi, l’accent croissant mis sur l’utilisation d’essais cliniques décentralisés et hybrides par rapport aux méthodes d’essais cliniques traditionnelles devrait offrir des opportunités lucratives pour le marché des essais cliniques au cours de la période de prévision.
Analyse de segmentation du rapport sur le marché des essais cliniques
Les segments clés qui ont contribué à l’élaboration de l’analyse du marché des essais cliniques sont la conception de l’étude, les indications et la phase.
- Sur la base de la conception de l'étude, le marché des essais cliniques est divisé en essais interventionnels et essais à accès élargi. Le segment des essais interventionnels détenait une part de marché plus importante en 2023.
- Par indication, le marché est segmenté en maladies cardiovasculaires, affections oncologiques, troubles neurologiques, maladies auto-immunes/inflammations, gestion de la douleur, diabète, obésité, troubles métaboliques et autres. Le segment des affections oncologiques détenait la plus grande part de marché en 2023.
- En fonction de la phase, le marché des essais cliniques est divisé en phase I, phase II et phase III. Le segment de la phase II détenait la plus grande part de marché en 2023.
Analyse des parts de marché des essais cliniques par zone géographique
La portée géographique du rapport sur le marché des essais cliniques est principalement divisée en cinq régions : Amérique du Nord, Asie-Pacifique, Europe, Amérique du Sud et centrale, et Moyen-Orient et Afrique. L'Amérique du Nord a dominé le marché en 2023. Les États-Unis sont le marché le plus important et celui qui connaît la croissance la plus rapide pour les essais cliniques. Les États-Unis sont en train de devenir une destination de premier plan pour la recherche clinique et diverses entreprises proposent des services d'essais cliniques innovants. Les États-Unis sont devenus une destination de premier plan pour la recherche clinique. Près de la moitié des essais cliniques sont menés aux États-Unis. De plus, la plupart des sociétés de recherche pharmaceutique préfèrent mener des essais cliniques dans le pays en raison de l'infrastructure médicale établie, des délais d'approbation rapides, d'un cadre réglementaire favorable et des données générées par les essais cliniques acceptées à l'échelle mondiale. Un rapport de l'Organisation mondiale de la santé (OMS) indique que les États-Unis ont enregistré le plus grand nombre d'essais cliniques, avec 157 618 essais en 2021.
Aperçu régional du marché des essais cliniques
Les tendances et facteurs régionaux influençant le marché des essais cliniques tout au long de la période de prévision ont été expliqués en détail par les analystes d’Insight Partners. Cette section traite également des segments et de la géographie du marché des essais cliniques en Amérique du Nord, en Europe, en Asie-Pacifique, au Moyen-Orient et en Afrique, ainsi qu’en Amérique du Sud et en Amérique centrale.
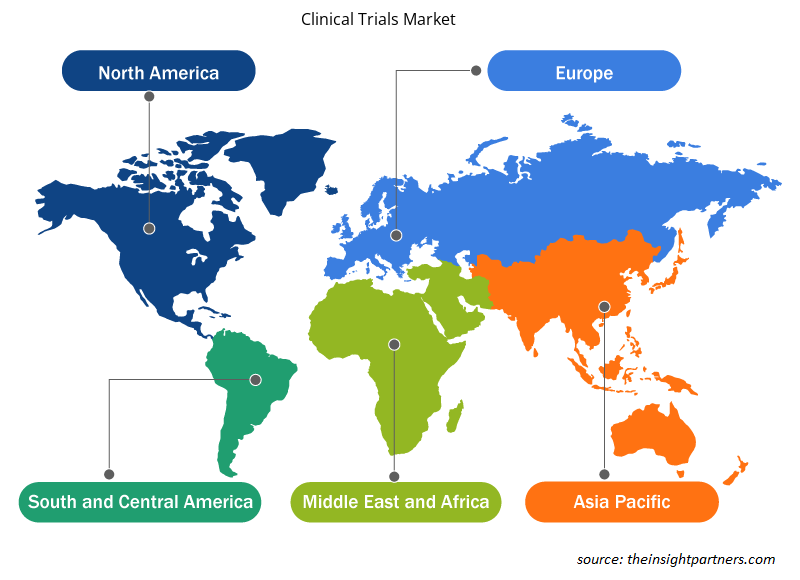
- Obtenez les données régionales spécifiques au marché des essais cliniques
Portée du rapport sur le marché des essais cliniques
| Attribut de rapport | Détails |
|---|---|
| Taille du marché en 2023 | 43,37 milliards de dollars américains |
| Taille du marché d'ici 2031 | 73,33 milliards de dollars américains |
| Taux de croissance annuel composé mondial (2023-2031) | 6,8% |
| Données historiques | 2021-2022 |
| Période de prévision | 2024-2031 |
| Segments couverts | Par conception d'étude
|
| Régions et pays couverts | Amérique du Nord
|
| Leaders du marché et profils d'entreprises clés |
|
Densité des acteurs du marché : comprendre son impact sur la dynamique des entreprises
Le marché des essais cliniques connaît une croissance rapide, tirée par la demande croissante des utilisateurs finaux en raison de facteurs tels que l'évolution des préférences des consommateurs, les avancées technologiques et une plus grande sensibilisation aux avantages du produit. À mesure que la demande augmente, les entreprises élargissent leurs offres, innovent pour répondre aux besoins des consommateurs et capitalisent sur les tendances émergentes, ce qui alimente davantage la croissance du marché.
La densité des acteurs du marché fait référence à la répartition des entreprises ou des sociétés opérant sur un marché ou un secteur particulier. Elle indique le nombre de concurrents (acteurs du marché) présents sur un marché donné par rapport à sa taille ou à sa valeur marchande totale.
Les principales entreprises opérant sur le marché des essais cliniques sont :
- IQVIA Holdings Inc
- Société Parexel International
- IXICO SA
- Laboratoires Charles River Inc.
- Icône Plc
- WuXi AppTec Co Ltd
Avis de non-responsabilité : les sociétés répertoriées ci-dessus ne sont pas classées dans un ordre particulier.
- Obtenez un aperçu des principaux acteurs du marché des essais cliniques
Actualités et développements récents du marché des essais cliniques
Le marché des essais cliniques est évalué en collectant des données qualitatives et quantitatives après des recherches primaires et secondaires, qui comprennent des publications d'entreprise importantes, des données d'association et des bases de données. Quelques-unes des évolutions du marché sont énumérées ci-dessous :
- Oracle a annoncé de nouvelles fonctionnalités dans Oracle Clinical One Randomization and Trial Supply Management (RTSM). Grâce à de nouvelles améliorations en termes d'utilisation, d'accès et de régionalisation, les utilisateurs de Clinical One RTSM peuvent répondre aux exigences réglementaires dynamiques et spécifiques à chaque pays et gagner en rapidité, en fiabilité et en transparence dans les essais, du début à la fin. (Source : Oracle Corp, site Web de la société, mai 2024)
- Parexel et Palantir Technologies Inc., un important constructeur de systèmes d'intelligence artificielle (IA), ont conclu un partenariat stratégique pluriannuel visant à exploiter l'IA pour contribuer à des essais cliniques améliorés, accélérés, sûrs et efficaces dans le monde entier. Dans le cadre de cette collaboration, Parexel s'appuie sur la Foundry et la plateforme d'intelligence artificielle (AIP) de Palantir pour alimenter sa plateforme de données cliniques axée sur l'amélioration de l'efficacité des essais cliniques tout en maintenant le plus haut niveau de sécurité et de rigueur réglementaire. (Source : Parexel International Corp, site Web de la société, avril 2024)
Rapport sur le marché des essais cliniques : couverture et livrables
Le rapport « Taille et prévisions du marché des essais cliniques (2021-2031) » fournit une analyse détaillée du marché couvrant les domaines ci-dessous :
- Taille et prévisions du marché des essais cliniques aux niveaux mondial, régional et national pour tous les segments de marché clés couverts par le périmètre
- Tendances du marché des essais cliniques, ainsi que la dynamique du marché, comme les facteurs moteurs, les contraintes et les opportunités clés
- Analyse PEST et SWOT détaillée
- Analyse du marché des essais cliniques couvrant les principales tendances du marché, le cadre mondial et régional, les principaux acteurs, les réglementations et les développements récents du marché
- Analyse du paysage industriel et de la concurrence couvrant la concentration du marché, l'analyse de la carte thermique, les principaux acteurs et les développements récents du marché des essais cliniques
- Profils d'entreprise détaillés
- Analyse historique (2 ans), année de base, prévision (7 ans) avec TCAC
- Analyse PEST et SWO
- Taille du marché Valeur / Volume - Mondial, Régional, Pays
- Industrie et paysage concurrentiel
- Ensemble de données Excel

Report Coverage
Revenue forecast, Company Analysis, Industry landscape, Growth factors, and Trends
Segment Covered
This text is related
to segments covered.

Regional Scope
North America, Europe, Asia Pacific, Middle East & Africa, South & Central America
Country Scope
This text is related
to country scope.
Questions fréquemment posées
IQVIA Holdings Inc, Parexel International Corporation, IXICO Plc, Charles River Laboratories Inc, ICON Plc, WuXi AppTec Co Ltd, SGS SA, Syneos Health Inc, SIRO Clinpharm Private Limited, Thermo Fisher Scientific Inc, Laboratory Corp of America Holdings, CliniRx, Caidya, Oracle Corp, and Medpace are among the key players in the market.
AI-driven clinical trials are expected to emerge as a prime trend in the market in the coming years.
The clinical trials market value is expected to reach US$ 73.33 billion by 2031.
The market is expected to register a CAGR of 6.8% during 2023–2031.
North America dominated the market in 2023.
The practice of outsourcing clinical studies with a massive rise in the number of trials and the flourishing pharmaceutical industry with a surge in R&D activities are among the most significant factors fueling the market growth.
Trends and growth analysis reports related to Life Sciences : READ MORE..
The List of Companies - Clinical Trials Market
- IQVIA Holdings Inc
- Parexel International Corp
- IXICO Plc
- Charles River Laboratories International Inc
- ICON Plc
- WuXi AppTec Co Ltd,
- SGS SA
- Syneos Health Inc
- SIRO Clinpharm Pvt Ltd
- Thermo Fisher Scientific Inc
The Insight Partners performs research in 4 major stages: Data Collection & Secondary Research, Primary Research, Data Analysis and Data Triangulation & Final Review.
- Data Collection and Secondary Research:
As a market research and consulting firm operating from a decade, we have published and advised several client across the globe. First step for any study will start with an assessment of currently available data and insights from existing reports. Further, historical and current market information is collected from Investor Presentations, Annual Reports, SEC Filings, etc., and other information related to company’s performance and market positioning are gathered from Paid Databases (Factiva, Hoovers, and Reuters) and various other publications available in public domain.
Several associations trade associates, technical forums, institutes, societies and organization are accessed to gain technical as well as market related insights through their publications such as research papers, blogs and press releases related to the studies are referred to get cues about the market. Further, white papers, journals, magazines, and other news articles published in last 3 years are scrutinized and analyzed to understand the current market trends.
- Primary Research:
The primarily interview analysis comprise of data obtained from industry participants interview and answers to survey questions gathered by in-house primary team.
For primary research, interviews are conducted with industry experts/CEOs/Marketing Managers/VPs/Subject Matter Experts from both demand and supply side to get a 360-degree view of the market. The primary team conducts several interviews based on the complexity of the markets to understand the various market trends and dynamics which makes research more credible and precise.
A typical research interview fulfils the following functions:
- Provides first-hand information on the market size, market trends, growth trends, competitive landscape, and outlook
- Validates and strengthens in-house secondary research findings
- Develops the analysis team’s expertise and market understanding
Primary research involves email interactions and telephone interviews for each market, category, segment, and sub-segment across geographies. The participants who typically take part in such a process include, but are not limited to:
- Industry participants: VPs, business development managers, market intelligence managers and national sales managers
- Outside experts: Valuation experts, research analysts and key opinion leaders specializing in the electronics and semiconductor industry.
Below is the breakup of our primary respondents by company, designation, and region:
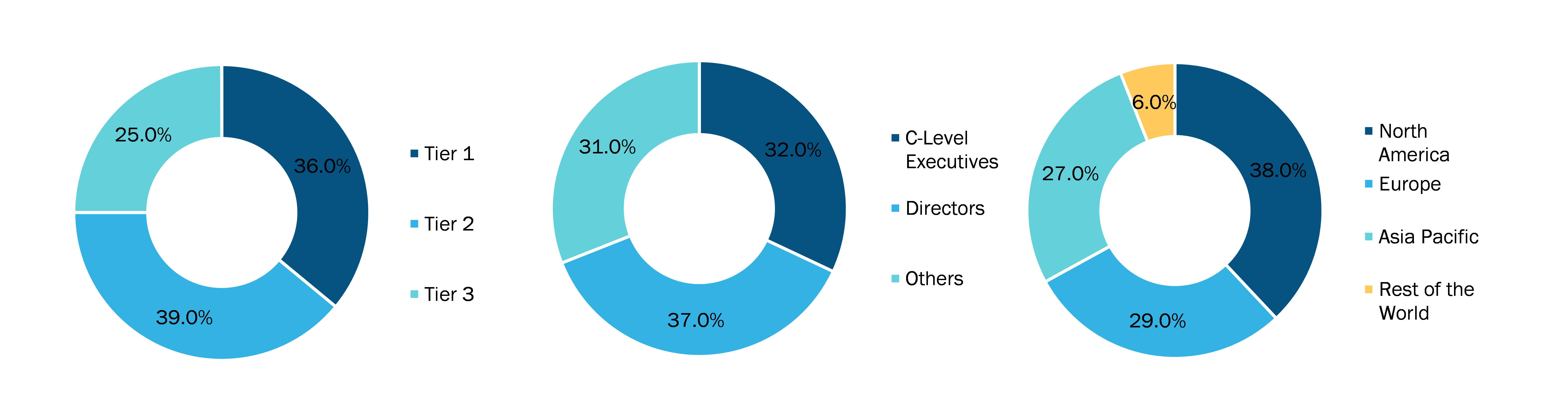
Once we receive the confirmation from primary research sources or primary respondents, we finalize the base year market estimation and forecast the data as per the macroeconomic and microeconomic factors assessed during data collection.
- Data Analysis:
Once data is validated through both secondary as well as primary respondents, we finalize the market estimations by hypothesis formulation and factor analysis at regional and country level.
- Macro-Economic Factor Analysis:
We analyse macroeconomic indicators such the gross domestic product (GDP), increase in the demand for goods and services across industries, technological advancement, regional economic growth, governmental policies, the influence of COVID-19, PEST analysis, and other aspects. This analysis aids in setting benchmarks for various nations/regions and approximating market splits. Additionally, the general trend of the aforementioned components aid in determining the market's development possibilities.
- Country Level Data:
Various factors that are especially aligned to the country are taken into account to determine the market size for a certain area and country, including the presence of vendors, such as headquarters and offices, the country's GDP, demand patterns, and industry growth. To comprehend the market dynamics for the nation, a number of growth variables, inhibitors, application areas, and current market trends are researched. The aforementioned elements aid in determining the country's overall market's growth potential.
- Company Profile:
The “Table of Contents” is formulated by listing and analyzing more than 25 - 30 companies operating in the market ecosystem across geographies. However, we profile only 10 companies as a standard practice in our syndicate reports. These 10 companies comprise leading, emerging, and regional players. Nonetheless, our analysis is not restricted to the 10 listed companies, we also analyze other companies present in the market to develop a holistic view and understand the prevailing trends. The “Company Profiles” section in the report covers key facts, business description, products & services, financial information, SWOT analysis, and key developments. The financial information presented is extracted from the annual reports and official documents of the publicly listed companies. Upon collecting the information for the sections of respective companies, we verify them via various primary sources and then compile the data in respective company profiles. The company level information helps us in deriving the base number as well as in forecasting the market size.
- Developing Base Number:
Aggregation of sales statistics (2020-2022) and macro-economic factor, and other secondary and primary research insights are utilized to arrive at base number and related market shares for 2022. The data gaps are identified in this step and relevant market data is analyzed, collected from paid primary interviews or databases. On finalizing the base year market size, forecasts are developed on the basis of macro-economic, industry and market growth factors and company level analysis.
- Data Triangulation and Final Review:
The market findings and base year market size calculations are validated from supply as well as demand side. Demand side validations are based on macro-economic factor analysis and benchmarks for respective regions and countries. In case of supply side validations, revenues of major companies are estimated (in case not available) based on industry benchmark, approximate number of employees, product portfolio, and primary interviews revenues are gathered. Further revenue from target product/service segment is assessed to avoid overshooting of market statistics. In case of heavy deviations between supply and demand side values, all thes steps are repeated to achieve synchronization.
We follow an iterative model, wherein we share our research findings with Subject Matter Experts (SME’s) and Key Opinion Leaders (KOLs) until consensus view of the market is not formulated – this model negates any drastic deviation in the opinions of experts. Only validated and universally acceptable research findings are quoted in our reports.
We have important check points that we use to validate our research findings – which we call – data triangulation, where we validate the information, we generate from secondary sources with primary interviews and then we re-validate with our internal data bases and Subject matter experts. This comprehensive model enables us to deliver high quality, reliable data in shortest possible time.

 Obtenez un échantillon gratuit pour ce rapport
Obtenez un échantillon gratuit pour ce rapport