Il mercato europeo del software per la farmacovigilanza e la sicurezza dei farmaci è stato valutato a 52,37 milioni di dollari nel 2023 e si prevede che raggiungerà gli 84,66 milioni di dollari entro il 2031; si stima che registrerà un CAGR del 6,2% nel periodo 2023-2031. È probabile che il software per la farmacovigilanza e la sicurezza dei farmaci basato su cloud introdurrà nuove tendenze chiave nel mercato nei prossimi anni.
Analisi del mercato europeo del software per la farmacovigilanza e la sicurezza dei farmaci
Il software di farmacovigilanza e sicurezza dei farmaci garantisce una rapida individuazione e valutazione delle reazioni avverse associate ai farmaci. Grazie al monitoraggio della sicurezza migliorato e all'automazione della raccolta e dell'analisi dei dati, il software accelera l'identificazione di potenziali problemi di sicurezza, consentendo un rapido intervento per mitigare i rischi. Questo approccio proattivo migliora la conformità normativa, la sicurezza dei pazienti e i risultati generali di salute pubblica. Inoltre, con la presenza di analisi avanzate e capacità di monitoraggio in tempo reale, il software di farmacovigilanza e sicurezza dei farmaci fornisce un solido quadro per ottimizzare la sorveglianza della sicurezza dei farmaci. L'integrazione di intelligenza artificiale e analisi predittiva con il software di farmacovigilanza e sicurezza dei farmaci migliora la capacità di identificare potenziali rischi per la sicurezza prima che si trasformino in problemi seri. Queste tecnologie avanzate aiutano ad analizzare grandi volumi di dati strutturati e non strutturati per rilevare segnali e tendenze di sicurezza imminenti, che innescano strategie proattive di mitigazione del rischio. Pertanto, grazie a vari vantaggi, la domanda di software di farmacovigilanza e sicurezza dei farmaci è in aumento in Europa.
Panoramica del mercato europeo del software per la farmacovigilanza e la sicurezza dei farmaci
La farmacovigilanza è la scienza che si occupa di preservare la salute pubblica garantendo la sicurezza e l'efficacia dei prodotti farmaceutici. Il software di farmacovigilanza e sicurezza dei farmaci è uno strumento essenziale che affronta gli errori di immissione manuale dei dati, l'enorme volume di dati sulla sicurezza e varie altre sfide. Dagli studi clinici alla sorveglianza post-marketing, questo software è indispensabile durante tutto il ciclo di vita dello sviluppo del farmaco. Il software di farmacovigilanza e sicurezza dei farmaci aiuta a ridurre i tempi di elaborazione degli eventi avversi e a migliorare la sicurezza dei pazienti attraverso il rilevamento precoce dei segnali. Con l'evoluzione delle normative e l'intensificarsi della collaborazione europea, l'adozione di software di farmacovigilanza e sicurezza dei farmaci è vantaggiosa, rendendola indispensabile per le aziende farmaceutiche e gli enti normativi. Nel 2022, il Pharmaceutical Inspection Co-operation Scheme (PIC/S) ha aggiornato le sue linee guida sulla farmacovigilanza per aderire agli standard internazionali, evidenziando l'importanza di un software di farmacovigilanza e sicurezza dei farmaci robusto. Inoltre, il software garantisce la conformità agli standard normativi facilitando la creazione di report di sicurezza completi e invii alle autorità di regolamentazione, il che aiuta le aziende a evitare sanzioni e a mantenere la propria reputazione.
Personalizza la ricerca in base alle tue esigenze
Possiamo ottimizzare e personalizzare l'analisi e l'ambito che non sono soddisfatti dalle nostre offerte standard. Questa flessibilità ti aiuterà a ottenere le informazioni esatte necessarie per la pianificazione aziendale e il processo decisionale.
Mercato europeo del software per la farmacovigilanza e la sicurezza dei farmaci: approfondimenti strategici
Tasso di crescita annuo composto (2023-2031)6,2%- Dimensione del mercato 2023
52,37 milioni di dollari USA - Dimensione del mercato 2031
84,66 milioni di dollari USA

Dinamiche di mercato
- Aumento dell'incidenza delle reazioni avverse ai farmaci
- Globalizzazione della farmacovigilanza
- Aumento dei tassi di sviluppo dei farmaci
- Farmacovigilanza basata sul cloud
- Software per la sicurezza dei farmaci
- Integrazione del software con AI, ML
- PNL
Giocatori chiave
- ArisEuropa
- ICON plc Salute Syneos
- Accentura
- IQVIA
- Genpact
- Cosciente
- Società internazionale Paraxel
- Società di laboratori di America Holdings
- Applicazione massima
- Tecnologie Clinevo
Panoramica regionale
- Europa
Segmentazione del mercato
 Offerta
Offerta- Software
- Servizi
 Distribuzione
Distribuzione- Nuvola
- In sede
 Dimensioni dell'impresa
Dimensioni dell'impresa- Grandi Imprese
- PMI
 Modulo
Modulo- Standard
- Personalizzato
- Il PDF di esempio illustra la struttura del contenuto e la natura delle informazioni con analisi qualitative e quantitative.
Driver e opportunità del mercato europeo del software per la farmacovigilanza e la sicurezza dei farmaci
Aumento dell'incidenza delle reazioni avverse ai farmaci
In Europa, le reazioni avverse ai farmaci (ADR) possono essere una causa significativa di morte e malattia. Poiché tutti i farmaci hanno il potenziale per causare reazioni avverse ai farmaci, è necessaria un'analisi rischio-beneficio ogni volta che un farmaco viene prescritto. Le ADR rimangono una sfida nell'assistenza sanitaria moderna, in particolare data la crescente complessità delle terapie, l'invecchiamento della popolazione e l'aumento della multimorbilità in Europa. Il software di farmacovigilanza consente agli operatori sanitari e alle aziende farmaceutiche di raccogliere, analizzare e segnalare sistematicamente i dati relativi alle ADR e di superare le sfide ad esse associate.
Le ADR sono una delle principali cause dell'aumento dei tassi di mortalità in Europa. Secondo il rapporto dell'Agenzia europea per le droghe (EUDA), in termini di overdose, il tasso di mortalità nell'Unione europea nel 2021 ha rappresentato circa 18,3 decessi per milione di abitanti di età compresa tra 15 e 64 anni. Inoltre, nel 2021 nell'Unione europea si sono verificati almeno 6.166 decessi causati da overdose di droghe illecite (5.796 nel 2020). Questo totale ha raggiunto circa 6.677 decessi se si includono Norvegia e Turchia (6.434 nel 2020).
Con la segnalazione e il riconoscimento di un numero sempre maggiore di ADR, le aziende farmaceutiche , gli operatori sanitari e gli enti normativi sono sottoposti a una pressione sempre maggiore per migliorare i processi di monitoraggio e segnalazione della sicurezza dei farmaci. Ciò richiede l'adozione di software di farmacovigilanza e sicurezza dei farmaci per raccogliere, analizzare e gestire il crescente volume di dati sulla sicurezza. Questo software aiuta a semplificare il processo di rilevamento, valutazione e prevenzione degli effetti avversi, consentendo tempi di risposta più rapidi e valutazioni del rischio più accurate. Pertanto, l'aumento delle incidenze di reazioni avverse ai farmaci alimenta la crescita del mercato europeo dei software di farmacovigilanza e sicurezza dei farmaci .
Integrazione del software con AI, ML e NLP
L'intelligenza artificiale (IA), l'apprendimento automatico (ML), l'elaborazione del linguaggio naturale (NLP) e altre tecnologie stanno trasformando i carichi di lavoro di farmacovigilanza ad alta intensità di risorse, garantendo un approccio più informato ed efficiente. Le piattaforme software di farmacovigilanza e sicurezza dei farmaci sono per lo più dotate di analisi avanzate e capacità di intelligenza artificiale che migliorano il rilevamento dei segnali di sicurezza. Questi strumenti possono analizzare grandi quantità di dati, identificando correlazioni e modelli che i metodi tradizionali potrebbero trascurare. L'analisi predittiva basata sull'intelligenza artificiale può anche prevedere potenziali problemi di sicurezza, consentendo alle aziende di adottare misure proattive. I modelli di ML vengono sfruttati per prevedere potenziali eventi avversi associati al consumo di farmaci. Ad esempio, le campagne di farmacovigilanza utilizzano l'ML per setacciare vasti set di dati, rilevando modelli che potrebbero indicare un rischio di reazioni avverse ai farmaci. Gli algoritmi di ML sono particolarmente abili nel gestire dati non strutturati, come i social media e le cartelle cliniche dei pazienti, per prevedere problemi di sicurezza.
I sistemi di intelligenza artificiale vengono progressivamente utilizzati per migliorare il monitoraggio della sicurezza dei farmaci in tempo reale. Questa sorveglianza proattiva include dati di sperimentazioni cliniche, scansione di letteratura medica e registri dei pazienti per eventi avversi (AE); può anche migliorare l'accuratezza e la velocità delle rilevazioni di ADR. Inoltre, utilizzando l'elaborazione del linguaggio naturale, i sistemi di intelligenza artificiale possono estrarre informazioni rilevanti, come nomi e sintomi dei farmaci, da vasti set di dati testuali, consentendo una segnalazione accurata e rapida degli eventi avversi. Ciò accelera l'identificazione di problemi di sicurezza dei farmaci sconosciuti o nuovi, migliorando così in modo significativo i progressi negli sforzi di farmacovigilanza. Diverse aziende offrono software di farmacovigilanza e sicurezza dei farmaci basati sull'intelligenza artificiale, tra cui ArisGlobal. Pertanto, si prevede che l'integrazione del software di farmacovigilanza e sicurezza dei farmaci con intelligenza artificiale, apprendimento automatico e elaborazione del linguaggio naturale creerà opportunità redditizie per la crescita del mercato durante il periodo di previsione.
Analisi della segmentazione del rapporto di mercato del software per la farmacovigilanza e la sicurezza dei farmaci in Europa
I segmenti chiave che hanno contribuito alla derivazione dell'analisi del mercato europeo del software per la farmacovigilanza e la sicurezza dei farmaci sono l'offerta, le dimensioni dell'organizzazione, l'implementazione, la forma, la funzionalità e l'utente finale.
- In base alle dimensioni dell'organizzazione, il mercato europeo del software per la farmacovigilanza e la sicurezza dei farmaci è diviso in grandi imprese e PMI. Il segmento delle grandi imprese ha dominato il mercato nel 2023.
- In termini di offerte, il mercato è diviso in software e servizi. Il segmento software ha detenuto una quota maggiore del mercato nel 2023.
- In base all'implementazione, il mercato europeo del software per la farmacovigilanza e la sicurezza dei farmaci è diviso in cloud e on-premise. Il segmento cloud ha dominato il mercato nel 2023
- In base alla forma, il mercato europeo del software per la farmacovigilanza e la sicurezza dei farmaci è suddiviso in standard e personalizzato. Il segmento standard ha dominato il mercato nel 2023.
- In base alla funzionalità, il mercato europeo del software per la farmacovigilanza e la sicurezza dei farmaci è suddiviso in gestione dei casi, gestione dei segnali e dei rischi, qualità e conformità, supporto di audit e conformità alla formazione, monitoraggio dei problemi e monitoraggio degli eventi avversi, gestione della sicurezza clinica e sicurezza degli studi clinici, redazione di documenti medici, analisi sanitarie e altri. Il segmento di gestione dei segnali e dei rischi ha detenuto la quota maggiore del mercato nel 2023.
- In base all'utente finale, il mercato europeo del software per la farmacovigilanza e la sicurezza dei farmaci è suddiviso in aziende farmaceutiche e biotecnologiche, organizzazioni di ricerca a contratto, aziende di esternalizzazione dei processi aziendali e altri fornitori di servizi di farmacovigilanza. Il segmento delle aziende farmaceutiche e biotecnologiche ha dominato il mercato nel 2023.
Analisi della quota di mercato del software per la farmacovigilanza e la sicurezza dei farmaci in Europa per area geografica
Il mercato europeo del software per la farmacovigilanza e la sicurezza dei farmaci è suddiviso in Francia, Germania, Italia, Spagna, Regno Unito e resto d'Europa. La crescente domanda di software per la farmacovigilanza e la sicurezza dei farmaci in Europa è attribuita a vari fattori, tra cui requisiti normativi, crescenti approvazioni di farmaci, crescente enfasi sulla sicurezza dei pazienti e progressi tecnologici. Il sistema di farmacovigilanza dell'UE è uno dei più avanzati al mondo. L'Agenzia europea per i medicinali (EMA) e altri enti normativi stanno imponendo severi requisiti di farmacovigilanza che richiedono l'adozione di soluzioni software avanzate. Ad esempio, l'introduzione della direttiva sulla farmacovigilanza dell'UE (2010/84/UE) e il successivo regolamento (UE) n. 1235/2010 hanno imposto regole più severe per il monitoraggio delle reazioni avverse ai farmaci (ADR). Le aziende devono segnalare i dati sulla sicurezza in tempo reale, aumentando significativamente la domanda di sistemi software efficienti in grado di gestire grandi volumi di dati.
Ambito del rapporto sul mercato europeo del software per la farmacovigilanza e la sicurezza dei farmaci
| Attributo del report | Dettagli |
|---|---|
| Dimensioni del mercato nel 2023 | 52,37 milioni di dollari USA |
| Dimensioni del mercato entro il 2031 | 84,66 milioni di dollari USA |
| CAGR globale (2023-2031) | 6,2% |
| Dati storici | 2021-2022 |
| Periodo di previsione | 2024-2031 |
| Segmenti coperti | Offrendo
|
| Regioni e Paesi coperti | Europa
|
| Leader di mercato e profili aziendali chiave |
|
- Il PDF di esempio illustra la struttura del contenuto e la natura delle informazioni con analisi qualitative e quantitative.
Notizie e sviluppi recenti sul mercato europeo del software per la farmacovigilanza e la sicurezza dei farmaci
Il mercato europeo del software per la farmacovigilanza e la sicurezza dei farmaci viene valutato raccogliendo dati qualitativi e quantitativi post-ricerca primaria e secondaria, che includono importanti pubblicazioni aziendali, dati di associazioni e database. Di seguito sono elencati alcuni degli sviluppi chiave nel mercato europeo del software per la farmacovigilanza e la sicurezza dei farmaci:
- ArisGlobal, leader di mercato nelle soluzioni tecnologiche per lo sviluppo di farmaci a livello globale, ha annunciato che Medac, un produttore farmaceutico tedesco specializzato nei settori dell'oncologia e dell'ematologia, dell'urologia e delle malattie autoimmuni, ha scelto LifeSphere Safety per modernizzare i suoi processi di sicurezza dei farmaci. Un'analisi precisa, specifica per paziente e popolazione, è fondamentale per ridurre al minimo i rischi di trattamento per i pazienti, il che supporta il miglior risultato di trattamento possibile. (Fonte: ArisGlobal, comunicato stampa, maggio 2023)
- IQVIA, fornitore leader a livello mondiale di analisi avanzate, soluzioni tecnologiche e servizi di ricerca clinica per il settore delle scienze biologiche, ha annunciato una collaborazione strategica con Argenx per migliorare il trattamento dei pazienti affetti da rare malattie autoimmuni attraverso servizi e soluzioni di sicurezza di farmacovigilanza (PV) innovativi e integrati basati sulla tecnologia. (Fonte: IQVIA, comunicato stampa, gennaio 2023)
Copertura e risultati del rapporto sul mercato europeo del software per la farmacovigilanza e la sicurezza dei farmaci
"Dimensioni e previsioni del mercato europeo del software per la farmacovigilanza e la sicurezza dei farmaci (2021-2031)" fornisce un'analisi dettagliata del mercato che copre le aree menzionate di seguito:
- Dimensioni e previsioni del mercato europeo dei software per la farmacovigilanza e la sicurezza dei farmaci a livello nazionale per tutti i segmenti di mercato chiave coperti dall'ambito
- Tendenze del mercato europeo dei software per la farmacovigilanza e la sicurezza dei farmaci, nonché dinamiche di mercato quali fattori trainanti, limitazioni e opportunità chiave
- Analisi PEST e SWOT dettagliate
- Analisi del mercato europeo dei software per la farmacovigilanza e la sicurezza dei farmaci che copre le principali tendenze del mercato, il quadro regionale, i principali attori, le normative e i recenti sviluppi del mercato
- Analisi del panorama industriale e della concorrenza che copre la concentrazione del mercato, l'analisi della mappa di calore, i principali attori e gli sviluppi recenti per il mercato europeo del software di farmacovigilanza e sicurezza dei farmaci
- Profili aziendali dettagliati
- Analisi storica (2 anni), anno base, previsione (7 anni) con CAGR
- Analisi PEST e SWOT
- Valore/volume delle dimensioni del mercato - Globale, regionale, nazionale
- Industria e panorama competitivo
- Set di dati Excel

Report Coverage
Revenue forecast, Company Analysis, Industry landscape, Growth factors, and Trends
Segment Covered
This text is related
to segments covered.

Regional Scope
North America, Europe, Asia Pacific, Middle East & Africa, South & Central America
Country Scope
This text is related
to country scope.
Domande frequenti
The Europe pharmacovigilance and drug safety software market was estimated to be US$ 52.37 million in 2023 and is expected to grow at a CAGR of 6.2% during the forecast period 2023 - 2031.
Cloud-based pharmacovigilance and drug safety software, which is anticipated to play a significant role in the Europe pharmacovigilance and drug safety software market in the coming years.
Rise in incidences of adverse drug reactions, globalization of pharmacovigilance, surge in drug development rates are the major factors that propel the Europe pharmacovigilance and drug safety software market.
The key players holding majority shares in the Europe pharmacovigilance and drug safety software market are ArisEurope, ICON plc, Syneos Health, Accenture, IQVIA, Genpact, Cognizant, Paraxel International Corporation, Laboratory Corporation of America Holdings, Max Application, Clinevo Technologies, Qinecsa Solutions, AB Cube, and Veeva Systems.
The incremental growth expected to be recorded for the Europe pharmacovigilance and drug safety software market during the forecast period is US$ 32.29 million.
The Europe pharmacovigilance and drug safety software market is expected to reach US$ 84.66 million by 2031.
Trends and growth analysis reports related to Technology, Media and Telecommunications : READ MORE..
The List of Companies - Europe Pharmacovigilance and Drug Safety Software Market
- ArisGlobal LLC
- Max Application
- Oracle Corp
- Veeva Systems Inc
- IQVIA Holdings Inc
- ICON Plc
- Cognizant Technology Solutions Corp
- Accenture Plc
- Syneos Health Inc
- Genpact Ltd.
- AB Cube S.A.S.
- Laboratory Corp of America Holdings
- Parexel International Corp
- Qinecsa Solutions
- Clinevo Technologies
The Insight Partners performs research in 4 major stages: Data Collection & Secondary Research, Primary Research, Data Analysis and Data Triangulation & Final Review.
- Data Collection and Secondary Research:
As a market research and consulting firm operating from a decade, we have published and advised several client across the globe. First step for any study will start with an assessment of currently available data and insights from existing reports. Further, historical and current market information is collected from Investor Presentations, Annual Reports, SEC Filings, etc., and other information related to company’s performance and market positioning are gathered from Paid Databases (Factiva, Hoovers, and Reuters) and various other publications available in public domain.
Several associations trade associates, technical forums, institutes, societies and organization are accessed to gain technical as well as market related insights through their publications such as research papers, blogs and press releases related to the studies are referred to get cues about the market. Further, white papers, journals, magazines, and other news articles published in last 3 years are scrutinized and analyzed to understand the current market trends.
- Primary Research:
The primarily interview analysis comprise of data obtained from industry participants interview and answers to survey questions gathered by in-house primary team.
For primary research, interviews are conducted with industry experts/CEOs/Marketing Managers/VPs/Subject Matter Experts from both demand and supply side to get a 360-degree view of the market. The primary team conducts several interviews based on the complexity of the markets to understand the various market trends and dynamics which makes research more credible and precise.
A typical research interview fulfils the following functions:
- Provides first-hand information on the market size, market trends, growth trends, competitive landscape, and outlook
- Validates and strengthens in-house secondary research findings
- Develops the analysis team’s expertise and market understanding
Primary research involves email interactions and telephone interviews for each market, category, segment, and sub-segment across geographies. The participants who typically take part in such a process include, but are not limited to:
- Industry participants: VPs, business development managers, market intelligence managers and national sales managers
- Outside experts: Valuation experts, research analysts and key opinion leaders specializing in the electronics and semiconductor industry.
Below is the breakup of our primary respondents by company, designation, and region:
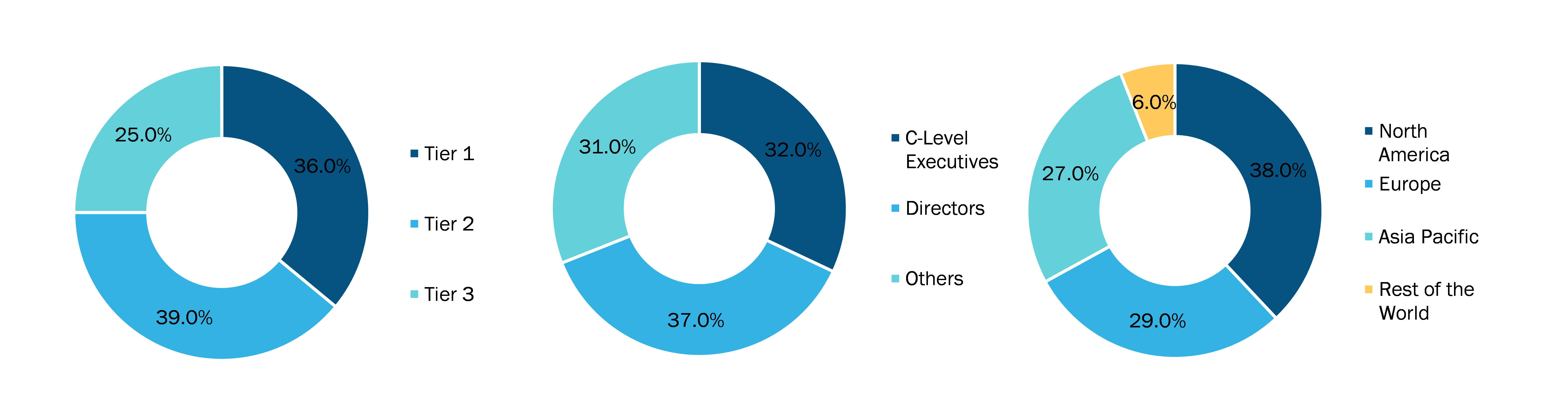
Once we receive the confirmation from primary research sources or primary respondents, we finalize the base year market estimation and forecast the data as per the macroeconomic and microeconomic factors assessed during data collection.
- Data Analysis:
Once data is validated through both secondary as well as primary respondents, we finalize the market estimations by hypothesis formulation and factor analysis at regional and country level.
- Macro-Economic Factor Analysis:
We analyse macroeconomic indicators such the gross domestic product (GDP), increase in the demand for goods and services across industries, technological advancement, regional economic growth, governmental policies, the influence of COVID-19, PEST analysis, and other aspects. This analysis aids in setting benchmarks for various nations/regions and approximating market splits. Additionally, the general trend of the aforementioned components aid in determining the market's development possibilities.
- Country Level Data:
Various factors that are especially aligned to the country are taken into account to determine the market size for a certain area and country, including the presence of vendors, such as headquarters and offices, the country's GDP, demand patterns, and industry growth. To comprehend the market dynamics for the nation, a number of growth variables, inhibitors, application areas, and current market trends are researched. The aforementioned elements aid in determining the country's overall market's growth potential.
- Company Profile:
The “Table of Contents” is formulated by listing and analyzing more than 25 - 30 companies operating in the market ecosystem across geographies. However, we profile only 10 companies as a standard practice in our syndicate reports. These 10 companies comprise leading, emerging, and regional players. Nonetheless, our analysis is not restricted to the 10 listed companies, we also analyze other companies present in the market to develop a holistic view and understand the prevailing trends. The “Company Profiles” section in the report covers key facts, business description, products & services, financial information, SWOT analysis, and key developments. The financial information presented is extracted from the annual reports and official documents of the publicly listed companies. Upon collecting the information for the sections of respective companies, we verify them via various primary sources and then compile the data in respective company profiles. The company level information helps us in deriving the base number as well as in forecasting the market size.
- Developing Base Number:
Aggregation of sales statistics (2020-2022) and macro-economic factor, and other secondary and primary research insights are utilized to arrive at base number and related market shares for 2022. The data gaps are identified in this step and relevant market data is analyzed, collected from paid primary interviews or databases. On finalizing the base year market size, forecasts are developed on the basis of macro-economic, industry and market growth factors and company level analysis.
- Data Triangulation and Final Review:
The market findings and base year market size calculations are validated from supply as well as demand side. Demand side validations are based on macro-economic factor analysis and benchmarks for respective regions and countries. In case of supply side validations, revenues of major companies are estimated (in case not available) based on industry benchmark, approximate number of employees, product portfolio, and primary interviews revenues are gathered. Further revenue from target product/service segment is assessed to avoid overshooting of market statistics. In case of heavy deviations between supply and demand side values, all thes steps are repeated to achieve synchronization.
We follow an iterative model, wherein we share our research findings with Subject Matter Experts (SME’s) and Key Opinion Leaders (KOLs) until consensus view of the market is not formulated – this model negates any drastic deviation in the opinions of experts. Only validated and universally acceptable research findings are quoted in our reports.
We have important check points that we use to validate our research findings – which we call – data triangulation, where we validate the information, we generate from secondary sources with primary interviews and then we re-validate with our internal data bases and Subject matter experts. This comprehensive model enables us to deliver high quality, reliable data in shortest possible time.
 Ottieni un campione gratuito per questo repot
Ottieni un campione gratuito per questo repot